题目内容
17.M是一种单质,A、B、C、D、E、F、G都是含有同一种元素的物质,这七种物质相互转变的关系如图所示: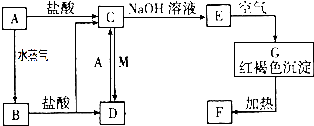
(1)写出下列物质的颜色:
M黄绿色 F红棕色,
(2)写出下列变化的化学方程式
A→B:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2该反应中每消耗0.3mol的A,可转移电子0.8 mol.
E→G:4Fe(OH)2+O2+2H2O=4 Fe(OH)3;
D→C:2FeCl3+Fe═3FeCl2.
(3)上述反应中,属于氧化还原反应的有5 个.
分析 M是一种单质,A、B、C、D、E、F、G都是含有同一种元素的物质,转化关系中依据反应现象判断,G为Fe(OH)3,加热分解得到F为Fe2O3,E为Fe(OH)2,C为FeCl2
,A和水蒸气反应生成B、与盐酸溶液反应生成FeCl2,判断A为Fe,B为Fe3O4,B溶于盐酸得到氯化亚铁和氯化铁,则D为FeCl3,M为Cl2,
(1)有颜色的物质是氯气为黄绿色、氧化铁为红棕色、氯化亚铁为浅绿色、氯化铁为黄色、氢氧化亚铁为白色、氢氧化铁为红褐色;
(2)A→B的反应是铁和水蒸气高温加热反应生成四氧化三铁和氢气,结合元素化合价和电子转移总数计算电子转移;
E→G是氢氧化亚铁被空气中的氧气氧化生成氢氧化铁;
D→C是铁和氯化铁溶液反应生成氯化亚铁;
(3)分析反应过程中有元素化合价变化的为氧化还原反应;
解答 解:M是一种单质,A、B、C、D、E、F、G都是含有同一种元素的物质,转化关系中依据反应现象判断,G为Fe(OH)3,加热分解得到F为Fe2O3,E为Fe(OH)2,C为FeCl2,A和水蒸气反应生成B、与盐酸溶液反应生成FeCl2,判断A为Fe,B为Fe3O4,B溶于盐酸得到氯化亚铁和氯化铁,则D为FeCl3,M为Cl2,
(1)有颜色的物质M是氯气为黄绿色气体,F为氧化铁为红棕色固体,
故答案为:黄绿色,红棕色;
(2)A→B的反应是铁和水蒸气高温加热反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,反应中每反应3molFe电子转移总数为8mol,该反应中每消耗0.3mol的A,计算电子转移为0.8mol,
故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,0.8;
E→G是氢氧化亚铁被空气中的氧气氧化生成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
D→C是铁和氯化铁溶液反应生成氯化亚铁,反应的化学方程式为:2FeCl3+Fe═3FeCl2,
故答案为:2FeCl3+Fe═3FeCl2;
(3)分析反应过程中有元素化合价变化的为氧化还原反应,A→B反应为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,是氧化还原反应,A→C的反应为Fe+2HCl=FeCl2+H2↑是氧化还原反应,C→D反应是2FeCl2+Cl2=3FeCl3是氧化还原反应,D→C反应是2FeCl3+Fe═3FeCl2,是氧化还原反应,E→G反应是4Fe(OH)2+O2+2H2O=4Fe(OH)3,是氧化还原反应,共有5个反应,
故答案为:5;
点评 本题考查了物质转化关系分析判断,主要是铁及其化合物性质,氧化还原反应的分析判断,注意反应现象判断和反应特征的理解应用是解题关键,题目难度中等.

 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | 硫离子的结构示意图: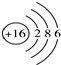 | |
| C. | H2O2的结构式:H-O-H-O | |
| D. | NH4I的电子式: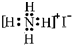 |
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |
| A. | FeO与稀硝酸反应:FeO+2H+═Fe2++H2O | |
| B. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32-+H+═HCO3- | |
| D. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 不法商家制取的“地沟油”具有固定的熔沸点 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 在家可用食醋代替CO2来增强漂白粉的漂白性 |
| A. | “地沟油”禁止食用,但可以用来制皂 | |
| B. | 安全、合理的使用核能有利于降低碳排放 | |
| C. | 采用“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| D. | 吸烟不会造成室内PM 2.5污染 |
| A. | H2O | B. | Na2O2 | C. | KClO3 | D. | KMnO4 |
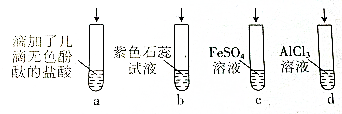
| A. | 若滴加过量的浓氨水,试管a中溶液由无色变红色 | |
| B. | 试管b中溶液由紫色变为蓝色 | |
| C. | 试管c中先有白色沉淀,后变为灰绿色,然后变为红褐色 | |
| D. | 试管d中先有白色沉淀,后白色沉淀消失 |