题目内容
10.下列由实验现象得出的结论一定正确的是( )| 操作及现象 | 结论 | |
| A | 向PbSO4悬浊液中加入KI溶液时出现黄色沉淀 | Ksp(PbI2)<Ksp(PbSO4) |
| B | 向某溶液中滴加氯水后再加入稀C6H5OH溶液,溶液呈红色 | 原溶液中可能含有Fe2+ |
| C | 向Na2SiO3溶液中通入过量SO2气体 | 反应为:SiO${\;}_{3}^{2-}$+SO2+H2O=H2SiO3↓+SO${\;}_{3}^{2-}$ |
| D | 将氢气还原氧化铜所得的红色固体加入足量稀硝酸中,溶液变为蓝色 | 反应为:3Cu+2NO${\;}_{3}^{-}$+8H+=3Cu2++2NO↑+4H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.向PbSO4悬浊液中加入KI溶液时出现黄色沉淀,发生沉淀的转化,生成Ksp小的物质;
B.原溶液在可能含铁离子;
C.向Na2SiO3溶液中通入过量SO2气体,反应生成硅酸和亚硫酸氢钠;
D.红色固体为Cu,Cu与稀硝酸反应生成硝酸铜.
解答 解:A.向PbSO4悬浊液中加入KI溶液时出现黄色沉淀,发生沉淀的转化,生成Ksp小的物质,则Ksp(PbI2)<Ksp(PbSO4),故A正确;
B.原溶液在可能含铁离子,应先加苯酚,后加氯水检验亚铁离子,故B错误;
C.向Na2SiO3溶液中通入过量SO2气体,反应生成硅酸和亚硫酸氢钠,则离子反应为SiO32-+2SO2+2H2O=H2SiO3↓+2HSO3-,故C错误;
D.红色固体为Cu,Cu与稀硝酸反应生成硝酸铜,溶液变为蓝色,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,把握沉淀转化、离子检验、物质的性质及反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
1.阿司匹林(主要成分为乙酰水杨酸)是解热止痛、治疗感冒的药物.它是由水杨酸(邻羟基苯甲酸)与醋酸酐进行酯化反应制得的.其反应原理如下:
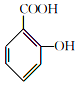 +
+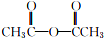 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$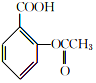 +CH3COOH
+CH3COOH
为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
制取阿司匹林的工艺流程如下:
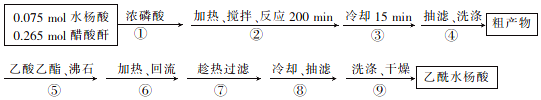
回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).
 +
+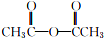 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$ +CH3COOH
+CH3COOH为避免醋酸酐水解,所用原料、仪器要充分干燥.有关物质的参数如表:
| 名称 | 式量 | 性质 | 熔点/℃ | 沸点/℃ | 溶解度 | ||
| 水 | 乙醇 | 乙酸乙酯 | |||||
| 水杨酸 | 138 | 白色结晶粉末、无臭 | 157~159 | 211 | 溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 无色液体、易燃、有醋酸味 | -73.1 | 138.6 | 易溶 | 溶 | 易溶 |
| 乙酸水杨酸 | 180 | 白色针状结晶 | 135 | 321.4 | 冰水微溶、热水可溶 | 易溶 | 微溶 |

回答下列问题:
(1)浓磷酸的作用是催化剂.步骤②的加热方式为水浴加热,温度控制在75~80℃.
(2)向粗产物中加入乙酸乙酯的作用是溶解水杨酸和醋酸酐等杂质,同时减少乙酰水杨酸因溶解而造成的损失.
(3)验证最后得到的乙酰水杨酸产品较为纯净的方法是测定产品熔点.
(4)精制后乙酰水杨酸的质量为8.91g,则其产率为66%,造成产率低的原因可能有反应温度没有控制好(或粗产品回流时的温度过高,造成产品水解发生副反应等)(任写一点).
18.下列A、B、C、D四个同学的陈述完全正确的是( )
| A. | NaCl:我是离子化合物,含有极性键 | |
| B. | H2O:我1mol中含有2mol非极性键 | |
| C. | KOH:既含有离子键,又含有极性共价键 | |
| D. | NaNO3:我是含有离子键的共价化合物 |
5.冰岛火山爆发再一次向人类敲响了警钟,必须发展“低碳经济”.氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车备思青睐.下列不是氢优点的是( )
| A. | 原料来源广 | B. | 易燃烧,放出热量多 | ||
| C. | 产物无污染 | D. | 制取H2简单易行 |
15.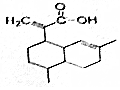 有机物X可作为合成青蒿素的一种基本原料,已知X的结构如图,下列有关X的说法正确的是( )
有机物X可作为合成青蒿素的一种基本原料,已知X的结构如图,下列有关X的说法正确的是( )
 有机物X可作为合成青蒿素的一种基本原料,已知X的结构如图,下列有关X的说法正确的是( )
有机物X可作为合成青蒿素的一种基本原料,已知X的结构如图,下列有关X的说法正确的是( )| A. | X为烃的含氧衍生物 | |
| B. | 1molX最多可以和3mol H2发生加成反应 | |
| C. | X只能发生取代反应和加成反应 | |
| D. | X可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同 |
2.氯化铁和氯化铜溶于足量水形成的溶液中含有0.8mol氯离子,且溶液中铜元素物质的量为铁元素的一半.现要使原溶液中的金属阳离子都转化为亚铁离子,需加铁粉( )
| A. | 5.6g | B. | 11.2g | C. | 16.8g | D. | 22.4g |
11.一种气态烷烃和一种气态烯烃组成的混合物共11.6g,混合气体的密度是相同状况下H2密度的14.5倍,该混合气体通过Br2水时,Br2水的质量增加8.4g,则组成该混合气体的可能是( )
| A. | 甲烷、乙烯 | B. | 乙烷、乙烯 | C. | 乙烷、丙烯 | D. | 甲烷、丙烯 |
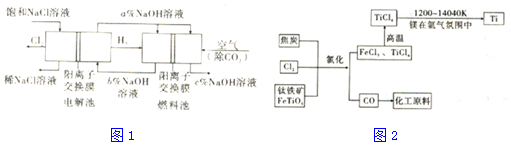
12.工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”.并能以它们为原料生产一系列化工产品.为提高原料的利用率,节能降耗.设计如图1所示工艺流程,其中氯碱工业装置中的电极未标出.
(1)电解饱和食盐水的化学方程式为2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是B (填序号).
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③C.①②④⑤③D.④②⑤
(3)图中NaOII溶液的质量分数a%、b%、c%,由大到小的顺序为c%>a%>b%.
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的四种钠盐溶液pH如表,下列说法不正确的是BD(填序号).
A.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐58.5t.
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图2.写出钛铁矿经氯化法得到四氯化钛的化学方程式:2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO.
(7)氮气和氩气是两种化学性质相对稳定的气体.镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气.试用化学反应方程式解释不选用氮气的原因:3Mg+N2$\frac{\underline{\;高温\;}}{\;}$Mg3N2.

(1)电解饱和食盐水的化学方程式为2Cl-+2H2$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
(2)为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,正确的操作步骤的顺序是B (填序号).
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④①②⑤③B.①②⑤④①③C.①②④⑤③D.④②⑤
(3)图中NaOII溶液的质量分数a%、b%、c%,由大到小的顺序为c%>a%>b%.
(4)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐.已知常温下,浓度均为0.1mol/L的四种钠盐溶液pH如表,下列说法不正确的是BD(填序号).
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
B.四种溶液中,水的电离程度最大的是NaClO
C.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是HClO
D.四种盐的阴离子结合H+能力最强的是HCO3-
(5)若利用电解氯化钠溶液所得的气体制36.5%的浓盐酸100t,最少需要消耗食盐58.5t.
(6)氯碱工业产品Cl2可用于冶炼钛铁矿得到金属钛,流程如图2.写出钛铁矿经氯化法得到四氯化钛的化学方程式:2FeTiO3+6C+7Cl2=2FeCl3+2TiCl4+6CO.
(7)氮气和氩气是两种化学性质相对稳定的气体.镁还原TiCl4的反应中为防止Mg和Ti被氧化选择稀有气体氩气.试用化学反应方程式解释不选用氮气的原因:3Mg+N2$\frac{\underline{\;高温\;}}{\;}$Mg3N2.