题目内容
20.同温同压下,相同体积的SO2和H2S气体的分子数之比是1:1,质量之比是32:17,密度之比是32:17.两种气体等体积混合后的平均摩尔质量是49g/mol,该混合气体对氢气的相对密度是24.5.同温同压下,相同质量的SO2和H2S气体的分子数之比是17:32,体积之比是17:32,所含原子数之比17:32.分析 根据阿伏加德罗定律可知,同温同压下同体积的SO2和H2S的物质的量相同,根据分子的组成和分子的相对分子质量计算粒子个数以及质量、密度等关系.由此分析解答.
解答 解:同温同压下,相同体积的SO2和H2S的物质的量相同,所以气体的分子数之比是1:1,等物质量的两种气体质量之比摩尔质量之比,质量之比为:64:34=32:17,相同体积的两种气体密度之比等于质量之比32:17,两种气体等体积混合后的平均摩尔质量是$\frac{64+34}{2}$=49g/mol,该混合气体对氢气的相对密度是$\frac{49}{2}$=24.5,同温同压下,相同质量的SO2和H2S气体的分子数之比是$\frac{1}{64}:\frac{1}{34}$=17:32;体积之比等于分子数之比是17:32;所含原子数之比17×3:32×3=17:32,
故答案为:1:1;32:17;32:17;49g/mol;24.5;17:32;17:32;17:32.
点评 本题考查物质的量有关计算,题目基础性强,贴近教材,有利于基础知识的巩固.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
2.如图所示原电池装置中,电解质溶液为稀盐酸,下列有关叙述错误的是( )
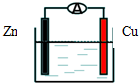

| A. | 锌做正极发生还原反应 | |
| B. | 供电时的总反应为:Zn+2H+=Zn2++H2 | |
| C. | 该装置可实现化学能转化为电能 | |
| D. | 产生1molH2,消耗锌的质量65g |
10.下列说法错误的是( )
| A. | 向苦卤(含K+、Mg2+、Br-等)中通入Cl2是为了提取溴 | |
| B. | 粗盐(含Ca2+、Mg2+、SO42-、泥沙等杂质)可采用除杂和重结晶等过程提纯 | |
| C. | 海带提碘只涉及物理变化,海水提镁涉及复分解反应 | |
| D. | 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收 |
11.下列有关实验描述说法正确的是( )
| 选项 | 实验描述 |
| A | 将SO2通入到紫色石蕊溶液中,溶液先变红后褪色 |
| B | 将SO2通入到KMnO4(H+)溶液中,紫色褪去 |
| C | 将Cl2与SO2 按物质的量之比1:1混合后,通入到品红溶液中,红色褪去 |
| D | 将CO2通入BaCl2溶液,出现白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
8.关于如图所示原电池的说法正确是 ( )
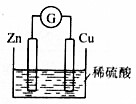

| A. | 锌电极是正电极 | B. | 锌电极得到电子 | ||
| C. | 铜电极上有氢气产生 | D. | 铜电极上发生氧化反应 |
15.发射“天宫一号”使用的燃料是偏二甲肼(用符号R表示),同时用四氧化二氮为氧化剂,两种物质混合便会剧烈燃烧,产生大量气体并释放出大量的热,该反应的化学方程式为:2N2O4+R→3N2+2CO2+4H2O,则R的化学式是( )
| A. | C3H5O | B. | C2H8N2 | C. | C2H8 | D. | C2H5N |
5.在0.1mol/L NH4Cl溶液中,离子浓度最大的是( )
| A. | Cl- | B. | NH4+ | C. | H+ | D. | OH- |
12.下列说法正确的是( )
| A. | 酸性氧化物一定是非金属氧化物 | B. | 碱性氧化物一定是金属氧化物 | ||
| C. | 氧气和臭氧是氧元素的不同核素 | D. | H2 D2 T2 互为同位素 |
1.CoO是电子陶瓷所需的重要原料,工业上可用含有Co2O3、Fe2O3、Li和Al等物质的废料制备CoO.生产流程如图:

已知:①Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
(1)为提高碱溶速率,除适当增大NaOH溶液浓度、提高反应温度外,还可采取的措施有将废料研磨成更小颗粒.
(2)步骤Ⅱ中酸溶时发生了反应:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O,此反应的目的是溶解Co2O3,将三价钴转化为Co2+,便于沉淀除去Fe3+.
(3)步骤Ⅲ中加入Na2CO3溶液的作用是调节溶液的pH,物质X的化学式为Fe(OH)3.
(4)步骤Ⅲ中加入NaF对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅵ中产生Li2CO3沉淀.
(5)操作A的步骤为过滤、洗涤、干燥,将所得的草酸钴晶体高温灼烧,其热重分析图如图:写出B点物质的化学式:CoO,CD段发生反应的化学方程式为:6CoO+O2=2Co3O4.
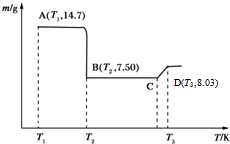

已知:①Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(2)步骤Ⅱ中酸溶时发生了反应:Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O,此反应的目的是溶解Co2O3,将三价钴转化为Co2+,便于沉淀除去Fe3+.
(3)步骤Ⅲ中加入Na2CO3溶液的作用是调节溶液的pH,物质X的化学式为Fe(OH)3.
(4)步骤Ⅲ中加入NaF对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅵ中产生Li2CO3沉淀.
(5)操作A的步骤为过滤、洗涤、干燥,将所得的草酸钴晶体高温灼烧,其热重分析图如图:写出B点物质的化学式:CoO,CD段发生反应的化学方程式为:6CoO+O2=2Co3O4.
