题目内容
铝不易被腐蚀,其主要原因是( )
| A、铝是一种轻金属 |
| B、铝的金属活动性比镁弱 |
| C、铝具有较高熔点 |
| D、铝易形成致密的氧化物薄膜 |
考点:铝的化学性质
专题:元素及其化合物
分析:金属铝能在空气中与氧气反应形成一层致密的保护层,防止铝进一步与氧气发生反应,致使铝制品不易被腐蚀,据此分析解答.
解答:
解:铝活动性较强,在常温下即能与氧气发生反应,反应的化学方程式为4Al+3O2═2Al2O3,在铝表面形成一层致密的氧化铝薄膜隔绝铝与氧气的接触,不易被腐蚀,
故选D.
故选D.
点评:本题主要考查了铝的化学性质,了解铝的性质化学性质活泼,易与氧气反应,在铝表面形成一层致密的氧化铝薄膜隔绝铝与氧气的接触是解答的关键,题目难度不大.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、碳酸氢钙溶液跟稀盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ |
| B、碳酸钙溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、饱和石灰水跟稀硝酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| D、氯化铁溶液中加入过量的铁粉:Fe3++Fe=Fe 2+ |
| E、向稀氨水中加入稀盐酸:NH3?H2O+H+=NH4++H2O |
| F、小苏打溶液个烧碱溶液反应:HCO3-+OH-=CO32-+H2O |
| G、氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO42-═H2O+BaSO4↓ |
| H、铁和稀硫酸反应:2Fe+3H+═2Fe3++3H2↑ |
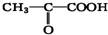 ),由以上事实推知乳酸的结构简式为
),由以上事实推知乳酸的结构简式为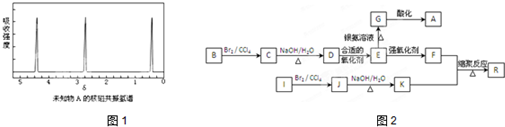
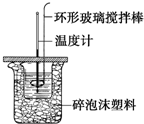 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下: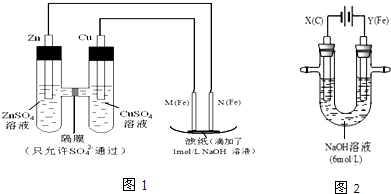
 对如图的解读不正确的是( )
对如图的解读不正确的是( )