题目内容
常温下的下列溶液,有关说法正确的是( )
| A、某酸H2A的钠盐NaHA溶液中:c(A2-)<c(H2A),则该溶液的pH>7 |
| B、1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 |
| C、在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| D、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
考点:pH的简单计算,盐类水解的原理
专题:
分析:A、HA-既电离又水解:HA-?H++A2-,HA-+H2O?H2A+OH-;
B、根据常温下酸溶液的pH一定小于7来分析;
C、根据离子对氨水的电离平衡的影响来分析平衡移动及溶液的pH;
D、HCO3-能电离和水解,CO32-有两步水解;
B、根据常温下酸溶液的pH一定小于7来分析;
C、根据离子对氨水的电离平衡的影响来分析平衡移动及溶液的pH;
D、HCO3-能电离和水解,CO32-有两步水解;
解答:
解:A、HA-既电离又水解:HA-?H++A2-,HA-+H2O?H2A+OH-,由于c(A2-)<c(H2A),说明HA-的水解程度大于电离程度,故溶液呈碱性,即该溶液的pH>7,故A正确;
B、因常温下,中性溶液的pH=7,则酸的pH一定小于7,即盐酸溶液的pH不会为8,故B错误;
C、在氨水中存在电离平衡,当加入NH4Cl,平衡逆向移动,氢氧根离子的浓度减小,由酚酞的变色范围8.2~10可知,此时溶液的pH可能小于8.2,不一定小于7,故C错误;
D、HCO3-能电离和水解,电离生成CO32-和H+,水解生成H2CO3和OH-,CO32-第一步水解生成HCO3-和OH-,第二步水解生成H2CO3和OH-,溶液中还存在H+,所以两种溶液中粒子种类相同,故D错误;
故选A.
B、因常温下,中性溶液的pH=7,则酸的pH一定小于7,即盐酸溶液的pH不会为8,故B错误;
C、在氨水中存在电离平衡,当加入NH4Cl,平衡逆向移动,氢氧根离子的浓度减小,由酚酞的变色范围8.2~10可知,此时溶液的pH可能小于8.2,不一定小于7,故C错误;
D、HCO3-能电离和水解,电离生成CO32-和H+,水解生成H2CO3和OH-,CO32-第一步水解生成HCO3-和OH-,第二步水解生成H2CO3和OH-,溶液中还存在H+,所以两种溶液中粒子种类相同,故D错误;
故选A.
点评:本题考查盐的水解的应用,明确水解原理及盐类水解规律的应用是解题的关键,难度不大.

练习册系列答案
相关题目
下列物质不属于天然高分子化合物的是( )
| A、淀粉 | B、纤维素 |
| C、油脂 | D、蛋白质 |
室温下,0.1mol/L氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是 ①电离度增大 ②C(OH-)增大 ③C(H+]增大 ④KW 增大⑤导电性增强 ⑥
增大( )
| c(OH-) |
| c(NH3?H2O) |
| A、①②③ | B、①③⑤ |
| C、①③⑥ | D、②④⑥ |
下列有关氯水的叙述,正确的是( )
| A、新制氯水可使无色酚酞试纸先变红,后褪色 |
| B、新制的氯水只含Cl2和H2O分子 |
| C、氯水放置数天后,酸性增强 |
| D、光照氯水有气泡逸出,该气体是Cl2 |
下列推断合理的是( )
| A、Fe3+、O2、H2O2三种微粒都具有氧化性,没有还原性 |
| B、木炭与浓硝酸反应可能生成CO和NH4NO3 |
| C、因为SO2具有还原性,所以不能用浓H2SO4干燥SO2 |
| D、Cl2转变为HClO时一定需要加入氧化剂才能实现 |
下列有关化学用语正确的是( )
A、O原子的电子排布图为 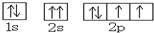 |
| B、氯化钠的分子式:NaCl |
C、Cl-的结构示意图: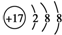 |
| D、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
下列反应的离子方程式不正确的是( )
| A、用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O |
| B、Fe跟稀硫酸反应:Fe+2H+=Fe2++H2↑ |
| C、澄清石灰水跟稀盐酸:H++OH-=H2O |
| D、碳酸氢钠溶液跟氢氧化钠溶液反应 HCO3-+OH-=H2O+CO2↑ |
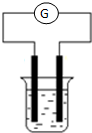 现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下: