题目内容
在同温同压下,用等质量的H2、CH4、CO2、HCl四种气体分别吹起四个气球,其中是由CO2吹起的是( )
A、 |
B、 |
C、 |
D、 |
考点:气体摩尔体积
专题:
分析:等质量的H2、CH4、CO2、HCl四种气体的物质的量与其摩尔质量成反比,即摩尔质量越大,则物质的量越小,在同温同压下,体积越小,据此解答.
解答:
解:气体的物质的量n=
,在同温同压下,气体摩尔体积相同,气体的体积V=n?Vm,即V=
Vm可知,摩尔质量越大,体积越小.H2、CH4、CO2、HCl的摩尔质量分别为2g/mol、16g/mol、44g/mol、36.5g/mol,CO2的摩尔质量最大,故体积最小,故答案为D.
故选D.
| m |
| M |
| m |
| M |
故选D.
点评:根据气体的物质的量、体积的计算公式来计算,难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、液态氯化氢、固体氯化钾均不导电,故HCl和KCl均为非电解质 |
| B、SO2、SO3水溶液都能导电,故二者均为电解质 |
| C、铜和石墨均能导电,所以它们都是电解质 |
| D、蔗糖、乙醇在水溶液中和熔融状态下都不导电,所以它们是非电解质 |
美国UIC大学两位国家级传染病学专家认为,当前形势的埃博拉病毒已经能够通过气溶胶传播.据此,下列说法正确的是( )
| A、埃博拉病毒无法通过呼吸传播 |
| B、佩戴口罩可有效预防埃博拉病毒侵染 |
| C、目前已找到有效治疗埃博拉病毒的方法 |
| D、埃博拉病毒颗粒直径大约80nm |
下列说法正确的是( )
| A、CH4的摩尔质量为16 |
| B、1 mol H2O的质量为18 g/mol |
| C、同温同压下,气体的密度与气体的相对分子质量成正比 |
| D、在相同温度条件下,气体分子间的平均距离几乎相等 |
以下化学用语正确的是( )
| A、H2SO4的电离方程式为:H2SO4=H2++SO4-2 |
| B、铁粉溶于盐酸的化学方程式:2Fe+6HCl=2FeCl3+3H2↑ |
C、氯离子的结构示意图: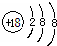 |
| D、乙醇的分子式为C2H6O |
下列说法中,正确的是( )
A、某原子(6个电子、7个中子)的化学符号是
| ||
| B、H2O和CH4分子中具有相同的质子数和原子数 | ||
| C、D和T是氢元素的两种不同的核素 | ||
| D、稀有气体的原子最外层达到稳定结构,故都不能与别的物质发生反应 |
下列化学用语正确的是( )
A、乙酸根离子的结构式: |
| B、3-甲基1-丁烯的结构简式:(CH3)2CHCH═CH2 |
| C、乙酸的结构简式C2H4O2 |
D、醛基的电子式: |
室温下对浓度,体积均相同的盐酸和醋酸溶液分别采取下列措施,有关叙述不正确的是( )
| A、醋酸溶液的PH值较大 |
| B、完全中和两溶液,需要浓度相同NaOH溶液的体积相等 |
| C、两者稀释相同倍数后,pH值变化相等 |
| D、加足量的锌充分反应后,两溶液中产生的氢气一样多 |