题目内容
14.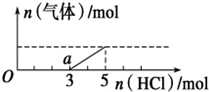 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )| A. | O点溶液中所含溶质的化学式为NaOH、Na2CO3 | |
| B. | a点溶液中c (HCO3-)>c (CO32-) | |
| C. | 标准状况下,通入CO2的体积为44.8L | |
| D. | 原NaOH溶液的物质的量浓度为5mol/L |
分析 a点进入与盐生成气体,发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,生成气体最大时消耗2mol HCl,可知碳酸氢钠为2mol,由Na2CO3+HCl=NaHCO3+NaCl,可知碳酸钠为2mol,碳酸钠转化为碳酸氢钠消耗2mol HCl,而图象中未生成二氧化碳时消耗的HCl为3mol,说明氢氧化钠溶液吸收二氧化碳后的溶液中还含有1mol NaOH,据此解答.
解答 解:a点进入与盐生成气体,发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,生成气体最大时消耗2mol HCl,可知碳酸氢钠为2mol,由Na2CO3+HCl=NaHCO3+NaCl,可知碳酸钠为2mol,碳酸钠转化为碳酸氢钠消耗2mol HCl,而图象中未生成二氧化碳时消耗的HCl为3mol,说明氢氧化钠溶液吸收二氧化碳后的溶液中还含有1mol NaOH.
A.由上述分析可知,O点溶液中所含溶质的化学式为NaOH、Na2CO3,故A正确;
B.a点为NaCl、NaHCO3混合溶液,溶液中HCO3-电离比较弱,故c (HCO3-)>c (CO32-)故B正确;
C.发生反应:NaHCO3+HCl=NaCl+H2O+CO2↑,生成气体最大时消耗2mol HCl,故二氧化碳为2mol,则标准状况下,通入CO2的体积为2mol×22.4L/mol=44.8L,故C正确;
D.加入5molHCl生成二氧化碳体积最大,此时溶液中溶质为NaCl,根据氯离子守恒有n(NaCl)=n(HCl),根据钠离子守恒有n(NaOH)=n(NaCl),故n(NaOH)=n(HCl)=5mL,所以c(NaOH)$\frac{5mol}{2L}$=2.5mol/L,故D错误.
故选:D.
点评 本题考查混合物的计算,难度中等,注意从图象分析反应发生的情况,关键是根据图象判断溶液溶质的成分,侧重考查学生分析计算能力.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案| 选项 | 实验操作 | 现象 | 结论 |
| A | 向1mL 0.1mol/LAgNO3溶液中滴加2滴0.1mol/LNaCl溶液,振荡后,再滴加2滴0.1mol/LKI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 加热盛有浓硫酸和可抽动铜丝的试管,并将产生的气体通入到品红溶液中 | 品红溶液褪色,且试管中只产生蓝色溶液 | 浓硫酸具有强氧化性 |
| C | 向丙烯醇(HOCH2CH=CH2)中滴入少量酸性高锰酸钾溶液 | 溶液紫红色褪去 | 丙烯醇中含有碳碳双键 |
| D | 碳酸钠溶液中滴加稀硫酸后,将产生的气体通入到硅酸钠溶液中 | 产生白色沉淀 | 非金属性:S>C>Si |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 向20mL1mol/L的FeBr2溶液中通入0.02molCl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 向漂白粉溶液中通入少量的SO2:SO2+Ca2++2ClO-+H2O═CaSO3↓+2HClO | |
| D. | 单质钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ |
| A. | 气态氢化物的稳定性:HX>H2Y>ZH3 | B. | 非金属活泼性:Y<X<Z | ||
| C. | 原子半径:X>Y>Z | D. | 原子最外层电子数:Z>Y>X |
| A. | 石墨 | B. | 液态HCl | C. | 葡萄糖 | D. | 熔融的Na2CO3 |
| A. | 液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 | |
| B. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 | |
| C. | 乙烯使高锰酸钾褪色和二氧化硫使溴水褪色的原理不相同 | |
| D. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 |
| A. | Na2O2与CO2 | B. | Na与O2 | C. | NaOH与CO2 | D. | NaAlO2与HNO3 |
| A. | NH4Al(SO4)2溶液与过量NaOH溶液反应:Al3++4OH-═AlO2-+2H2O | |
| B. | ICl溶于冷的稀KOH溶液中:ICl+2OH-═Cl-+IO-+H2O | |
| C. | 用惰性电极点解CuSO4溶液:2Cu2++4OH-$\frac{\underline{\;电解\;}}{\;}$2Cu↓+O2↑+2H2O | |
| D. | NaAlO2溶液中AlO2-的水解:AlO2-+2H2O═Al(OH)3+OH- |