题目内容
8.少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )①滴入几滴浓盐酸
②加NaCl溶液
③滴入几滴硫酸铜溶液
④升高温度(不考虑盐酸挥发)
⑤改用 18.4mol/L的硫酸溶液.
| A. | ①③④ | B. | ②④ | C. | ①④ | D. | ①④⑤ |
分析 可以通过增大盐酸浓度、升高温度等方法来改变,但改变条件时不能加入和稀盐酸反应生成氢气的物质,据此分析解答.
解答 解:①滴入几滴浓盐酸,氢离子浓度增大,反应速率加快,且生成氢气量不变,故正确;
②加NaCl溶液,氢离子浓度降低,反应速率减慢,故错误;
③滴入几滴硫酸铜溶液,Fe和铜离子发生置换反应生成Cu,Fe、Cu和稀盐酸构成原电池而加快反应速率,但生成氢气总量减小,故错误;
④升高温度(不考虑盐酸挥发),增大活化分子百分数,化学反应速率增大,且不影响生成氢气总量,故正确;
⑤改用 18.4mol/L的硫酸溶液,浓硫酸和Fe发生钝化现象,导致生成氢气总量减小,故错误;
故选C.
点评 本题考查化学反应速率影响因素,为高频考点,浓度、温度、催化剂、反应物接触面积、压强都是影响化学反应速率因素,注意这些外界条件的适用范围,注意:浓硫酸和Fe、Al易发生钝化现象,题目难度不大.

练习册系列答案
相关题目
16.下列物质中,不与水反应的是( )
| A. | Cl2 | B. | Na2O2 | C. | Na2O | D. | NaOH |
3.化学在生产、生活中有着广泛的应用,下列叙述不合理的是( )
| A. | 晶体硅熔点高,可制玻璃仪器 | B. | NaHCO3受热分解,可焙制糕点 | ||
| C. | N2化学性质稳定,可作保护气 | D. | 明矾易水解生成胶体,可作净水剂 |
13.中学常见的某反应化学方程式为X+Y→M+N+H2O(未配平,反应条件已略去),下列叙述错误的是( )
| A. | 若X、Y的物质的量之比为1:4,且N是黄绿色气体,则该反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 若M、N为气体,且都能使澄清石灰水变浑浊,则将此混合气体通入溴水中,橙色褪色,橙色褪色过程的离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br- | |
| C. | 若X是铁,Y是稀硝酸(过量),则X与Y反应的离子方程式为Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| D. | 当N为氯碱工业的主要原料,M是造成温室效应的主要气体,则上述反应的离子方程式一定为CO32-+2H+=CO2↑+H2O |
20.某实验小组设计如下实验装置探究电化学原理,装置Ⅰ中Zn电极产生ZnO,下列说法正确的是( )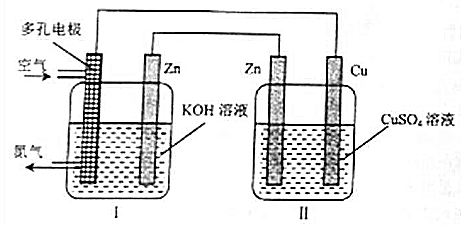

| A. | Cu电极质量增加 | |
| B. | 装置Ⅱ将化学能转变为电能 | |
| C. | 装置Ⅰ中OH-向多孔电极移动 | |
| D. | 多孔电极的电极反应式为:O2+4e-+2H2O═4OH- |
17.设NA为阿伏加徳罗常数的值.下列有关叙述正确的是( )
| A. | 1 mo1H2O分子所含中子数为8NA | |
| B. | 30g乙烷中所含的共价键数为6 NA | |
| C. | 常温下,1LpH=1的H2SO4溶液中,含有H+的数目为0.2 NA | |
| D. | 100 mL0.1mol•L-1的CuCl2溶液中,含有Cu2+的数目为0.01 NA |
2.某地海水中主要离子的含量如表:
利用电渗析法技术可将海水淡化,其原理如图所示,其中阴(阳)离子交换膜只允许阴(阳)离子通过,下列说法中不正确的是( )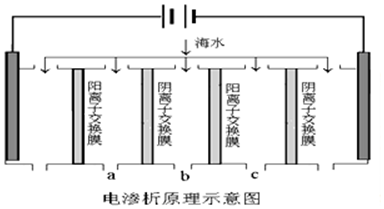
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含最/mg•L-1 | 9360 | 83 | 200 | 1100 | 16000 | 1200 | 118 |

| A. | 电解一段时间后阴极区会发生反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 阳极的电极反应式为2H2O-4e-═O2↑+4H+ | |
| C. | 电解时b室中阴离子移向a室,阳离子移向c室 | |
| D. | 淡水的出口为b出口 |
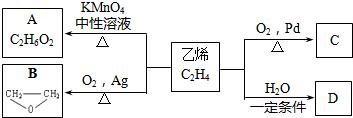
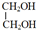 +2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
+2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.