题目内容
下列实验装置能够达到目的是( )
A、 检验溴乙烷在NaOH乙醇溶液加热的产物 |
B、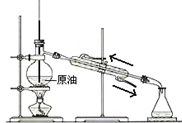 石油的分馏 |
C、 分离乙醇和乙酸的混合物 |
D、 实验室制取乙酸乙酯 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.溴乙烷在NaOH乙醇溶液加热,发生消去反应生成乙烯,水可除去乙烯中的乙醇;
B.分馏应测定馏分的温度,且冷却水应下进上出;
C.乙醇和乙酸的混合物不分层;
D.图中装置可制备乙酸乙酯,b中导管应在液面以上.
B.分馏应测定馏分的温度,且冷却水应下进上出;
C.乙醇和乙酸的混合物不分层;
D.图中装置可制备乙酸乙酯,b中导管应在液面以上.
解答:
解:A.溴乙烷在NaOH乙醇溶液加热,发生消去反应生成乙烯,水可除去乙烯中的乙醇,则高锰酸钾褪色可检验消去反应产物乙烯,故A正确;
B.由图可知,温度计的水银球应在蒸馏烧瓶的支管口处,且冷却水应下进上出,故B错误;
C.乙醇和乙酸的混合物不分层,不能利用分液分离,应利用蒸馏法分离,故C错误;
D.图中装置可制备乙酸乙酯,b中导管应在液面以上,长导管起冷凝回流作用,b中加饱和碳酸钠溶液,故D正确;
故选AD.
B.由图可知,温度计的水银球应在蒸馏烧瓶的支管口处,且冷却水应下进上出,故B错误;
C.乙醇和乙酸的混合物不分层,不能利用分液分离,应利用蒸馏法分离,故C错误;
D.图中装置可制备乙酸乙酯,b中导管应在液面以上,长导管起冷凝回流作用,b中加饱和碳酸钠溶液,故D正确;
故选AD.
点评:本题考查化学实验方案的评价,为高频考点,涉及有机物性质实验及制备实验、混合物分离提纯方法等,把握物质的性质及反应原理为解答的关键,侧重分析能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
下列各组物质属于同分异构体的是( )
| A、O2和O3 |
| B、H2O和H2O2 |
| C、正丁烷和异丁烷 |
| D、H和D |
将铁铝矾[Al2Fe(SO4)4?xH2O]溶于水中,得到浅绿色溶液,对该溶液的叙述正确的是( )
| A、铁铝矾有净水作用,其水溶液显中性 | ||||
B、该溶液中:2c(Al3+)+c(Fe2+)+c(H+)=
| ||||
| C、在空气中,蒸干并灼烧该溶液,最后所得的残留固体为Al2O3、Fe2O3 | ||||
| D、向该溶液中加入Ba(OH)2溶液,当SO42-完全沉淀时Al3+、Fe3+恰好被完全沉淀 |
下列关于物质的用途的叙述中,不正确的是( )
| A、石墨可以做绝缘材料 |
| B、硅可以做制造变压器的铁芯材料 |
| C、二氧化硅可以做光导纤维 |
| D、石英玻璃可以用来制造光学仪器 |
在一定温度下,向容积为1L的密闭容器中加入1mol A气体和2mol B气体,发生反应:A(g)+2B(g)?2C(g)下列说法,属于该反应达到平衡标志的是( )
| A、当2VA(逆)=VC(正)时 |
| B、单位时间每生成0.1mol B同时消耗0.1mol C |
| C、容器内气体的密度不随时间变化 |
| D、容器内A、B、C的浓度之比为1:2:2 |
下列各组微粒,氧化性按由强到弱的顺序排列的是( )
| A、Cu2+ H+ Zn2+ Fe2+ |
| B、Cu Fe Al Mg |
| C、F2 Cl2 Br2 I2 |
| D、F- Cl- Br- I- |
下列物质一定属于同系物的是( )


| A、④和⑥ | B、①和③ |
| C、②和⑤ | D、④和⑧ |
 X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:
X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知: