题目内容
 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:(1)用元素符号表示B、C、D三种元素的电负性由低到高的顺序
(2)C和D按原子个数比1:3形成的微粒其空间构型为
(3)E元素的+2价氧化物的熔点比+3价氧化物
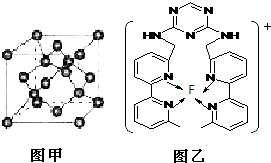
(4)B单质的一种同素异形体的晶胞如图甲所示,若晶体的密度为ρg/cm3,阿伏加德罗常数的值为NA,则晶体中最近的两个原子之间的距离为
(5)人工模拟酶是当前科技研究的热点,F离子是人体内多种酶的辅因子.
①F原子的外围电子排布式为
②某化合物与F(Ⅰ)(Ⅰ表示化合价为+1)结合形成图乙所示的离子:该离子中碳原子的杂化方式为
考点:位置结构性质的相互关系应用,晶胞的计算,原子轨道杂化方式及杂化类型判断
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,则A为H元素;B元素含有3个能级,且每个能级所含的电子数相同,原子核外电子排布为1s22s22p2,则B为C元素;D的原子核外有8个运动状态不同的电子,则D为O元素;C原子序数介于碳、氧之间,则C为N元素;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,应处于Ⅷ族及相邻的族,E元素的基态原子有4个未成对电子,外围电子排布为3d64s2,则E为Fe,故F为Cu,据此解答.
解答:
解:A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,则A为H元素;B元素含有3个能级,且每个能级所含的电子数相同,原子核外电子排布为1s22s22p2,则B为C元素;D的原子核外有8个运动状态不同的电子,则D为O元素;C原子序数介于碳、氧之间,则C为N元素;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,应处于Ⅷ族及相邻的族,E元素的基态原子有4个未成对电子,外围电子排布为3d64s2,则E为Fe,故F为Cu,
(1)同周期随原子序数增大,元素电负性增大,故电负性C<N<O,
故答案为:C<N<O;
(2)N和O按原子个数比1:3形成的微粒为NO3-,N原子价层电子对数=3+
=3、不含孤电子对,故其空间构型为平面三角形,
故答案为:平面三角形;
(3)Fe2+离子半径比Fe3+离子半径大,所带电荷少,故FeO晶格能比Fe2O3小,FeO的熔点比Fe2O3低,
故答案为:低;Fe2+离子半径比Fe3+离子半径大,所带电荷少,故FeO晶格能比Fe2O3小;
(4)晶胞中C原子数目=4+6×
+8×
=8,晶胞质量=8×
g=
g,若晶体的密度为ρg/cm3,则
晶胞体积=
=
cm3,则晶胞棱长=
cm,C原子与周围4个C原子形成正四面体,该正四面体的棱长=
cm×
=
×
cm,则晶体中最近的两个原子之间的距离=
cm,
故答案为:
;
(5)①F为Cu,原子的外围电子排布式为3d104s1 ,向CuSO4溶液中通入过量的NH3可生成[Cu(NH3)4]2+,再加入乙醇,会析出深蓝色晶体,其化学式为[Cu(NH3)4]SO4?H2O,
故答案为:3d104s1 ;[Cu(NH3)4]SO4?H2O;
②杂环上的碳原子含有3个σ键,没有孤对电子,采用sp2杂化,亚甲基上碳原子含有4个共价单键,采用sp3杂化,
故答案为:sp2、sp3.
(1)同周期随原子序数增大,元素电负性增大,故电负性C<N<O,
故答案为:C<N<O;
(2)N和O按原子个数比1:3形成的微粒为NO3-,N原子价层电子对数=3+
| 5+1-2×3 |
| 2 |
故答案为:平面三角形;
(3)Fe2+离子半径比Fe3+离子半径大,所带电荷少,故FeO晶格能比Fe2O3小,FeO的熔点比Fe2O3低,
故答案为:低;Fe2+离子半径比Fe3+离子半径大,所带电荷少,故FeO晶格能比Fe2O3小;
(4)晶胞中C原子数目=4+6×
| 1 |
| 2 |
| 1 |
| 8 |
| 12 |
| NA |
| 96 |
| NA |
晶胞体积=
| ||
| ρ g/cm3 |
| 96 |
| ρNA |
| 3 |
| ||
| 3 |
| ||
| ||
| 2 |
| 2 |
| 3 |
| ||
| |||||||
sin
|
故答案为:
| |||||||
sin
|
(5)①F为Cu,原子的外围电子排布式为3d104s1 ,向CuSO4溶液中通入过量的NH3可生成[Cu(NH3)4]2+,再加入乙醇,会析出深蓝色晶体,其化学式为[Cu(NH3)4]SO4?H2O,
故答案为:3d104s1 ;[Cu(NH3)4]SO4?H2O;
②杂环上的碳原子含有3个σ键,没有孤对电子,采用sp2杂化,亚甲基上碳原子含有4个共价单键,采用sp3杂化,
故答案为:sp2、sp3.
点评:本题是对物质结构的考查,涉及核外电子排布、电负性、配合物、杂化理论、晶胞计算等,(4)中计算为易错点、难点,需要学生理解晶胞结构,具备一定的空间想象与数学计算能力,注意理解均摊法进行晶胞有关计算,难度中等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
除去苯中的少量苯酚杂质的通常方法是( )
| A、加水振荡,静置分层后用分液漏斗分离 |
| B、加NaOH溶液振荡后,静置分液 |
| C、加溴水振荡后,过滤 |
| D、加CCl4振荡后,静置分液 |
 A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如图所示.A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )| A、简单离子的半径大小关系:B>C>E |
| B、D元素的气态氢化物比C元素的气态氢化物稳定 |
| C、由A、B、C三种元素组成的离子化合物NH4NO3中,阴、阳离子个数比为1:1 |
| D、由C、D、E三种元素组成的某种化合物,水解显碱性 |
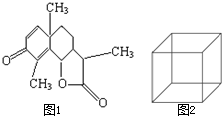 (1)图1是一种驱蛔虫药--山道年的结构简式,试确定其分子式为:
(1)图1是一种驱蛔虫药--山道年的结构简式,试确定其分子式为: