题目内容
11.0.01mol Al投入100mL 3mol•L-1 NaOH溶液中充分反应后,再滴入1mol•L-1 H2SO4 120mL,其结果( )| A. | 溶液的pH<7 | B. | 得到澄清透明溶液 | ||
| C. | 得到浑浊液 | D. | 先有白色沉淀生成,后逐渐溶解 |
分析 发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑、2NaOH+H2SO4=Na2SO4+H2O、H++AlO2-+H2O=Al(OH)3↓,n(Al)=0.01mol,n(NaOH)=0.1L×3mol/L=0.3mol,n(H+)=1mol/L×0.12L×2=0.24mol,以此来解答.
解答 解:n(Al)=0.01mol,n(NaOH)=0.1L×3mol/L=0.3mol,
由2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,Al完全反应,消耗NaOH为0.01mol,
由2NaOH+H2SO4=Na2SO4+H2O可知,0.29molNaOH需要硫酸为$\frac{0.29mol}{2}$=0.145mol,
而n(H+)=1mol/L×0.12L×2=0.24mol,硫酸为0.12mol,硫酸不足,则不发生H++AlO2-+H2O=Al(OH)3↓,
即溶液显碱性,得到得到澄清透明溶液,
故选B.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应、物质的量关系为解答的关键,侧重分析与计算能力的考查,注意反应中物质的量关系,题目难度不大.

练习册系列答案
相关题目
2.软锰矿(主要成分是MnO2)与过量KOH和KClO3固体在高温下反应,生成K2MnO4和KCl,其反应化学方程式为 MnO2+KOH+KClO3$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+KCl+H2O(未配平)下列说法中正确的是( )
| A. | 反应中MnO2是氧化剂 | |
| B. | 氧化产物与还原产物物质的量之比为1:3 | |
| C. | KClO3在反应中失去电子 | |
| D. | 反应中每生成l mol K2MnO4,氧化剂得到2 mol电子 |
19.除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| D | 溴苯(溴单质) | 苯 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
6.化合物丙是制备液晶材料的中间体之一,它可由甲和乙在一定条件下制得
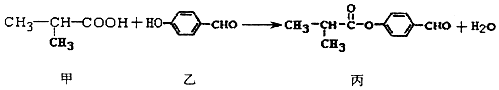
下列说法正确的是( )

下列说法正确的是( )
| A. | 丙的分子式为C11H11O3 | |
| B. | 甲分子中含有1个手性碳原子 | |
| C. | 乙、丙各lmol分别和氢气反应,最多消耗氢气均为4mol | |
| D. | 丙可发生加成反应、取代反应、氧化反应等 |
16.短周期元素A、B、C的原子序数依次递增,它们的原子最外层电子数之和为10,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,则下列叙述正确的是( )
| A. | 原子半径:A<B<C | |
| B. | 三种元素的最高价氧化物对应水化物均可由化合反应得到 | |
| C. | A的氢化物稳定性小于C的氢化物稳定性 | |
| D. | B 和A的最高价氧化物可发生置换反应 |
20.已知K2Cr2O7溶液中存在平衡:Cr2O72- (橙色)+H2O?2CrOr42- (黄色)+2H+保持温度不变,用k2O2O7溶液进行下列实验:结合实验,下列说法正确的是( )
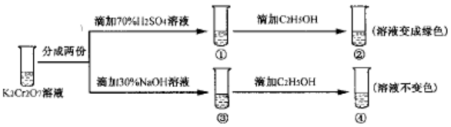

| A. | ①中溶液变黄,③中溶液橙色加深 | |
| B. | 上述可逆反应的平衡常数:①<③ | |
| C. | K2Cr2O7溶液的氧化性在酸性条件下更强 | |
| D. | 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 |
 NaHNa+[:H]- CsOH
NaHNa+[:H]- CsOH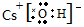 HSCN
HSCN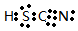 O22-
O22- .
.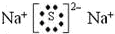 .
.