题目内容
14.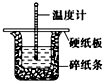 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
(2)大烧杯上如不盖硬纸板,求得的中和热△H偏小(填“偏大”“偏小”“无影响”).
(3)实验改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1NaOH溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),所求中和热相等(填“相等”、“不相等”).
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会偏小(填“偏大”“偏小”“无影响”).
(5)近似认为用0.50mol•L-1盐酸与0.55mol•L-1NaOH溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=4.18J•g-1•℃-1,若反应后温度升高4℃,则中和热为66.8kJ/mol.
分析 (1)根据量热计的构造来判断该装置的缺少仪器;
(2)大烧杯上如不盖硬纸板,会使一部分热量散失;
(3)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(4)根据弱电解质电离吸热分析;
(5)根据Q=m•c•△T计算出反应放出的热量,然后计算出生成1mol水放出的热量,就可以得到中和热.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;
故答案为:环形玻璃搅拌棒;
(2)大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
(3)反应放出的热量和所用酸以及碱的量的多少有关,改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以改用60mL 0.50mol•L-1盐酸跟50mL 0.55mol•L-1NaOH溶液进行实验,测得中和热数值相等;
故答案为:不相等;相等;
(4)氨水为弱碱,电离过程为吸热过程,所以用相同浓度和体积的氨水代替NaOH溶液反应,反应放出的热量偏小;
故答案为:偏小;
(5)50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液反应,生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为100mL×1g/cm3=100g,温度变化的值为△T=4℃,则生成0.025mol水放出的热量为:Q=m•c•△T=100g×4.18J/(g•℃)×4℃=1672J,即1.672KJ,所以实验测得的中和热△H=-$\frac{1.672KJ}{0.025mol}$=-66.8kJ/mol;
故答案为:66.8kJ/mol.
点评 本题考查了中和热的测定方法,题目难度中等,明确中和热的测定步骤为解答关键,注意掌握中和热计算方法,试题培养了学生的分析能力及化学实验能力.

| A. | 某酸性溶液中只含有Na+.CH3COO-.H+.OH-,向该溶液中加入适量氨水,c(CH3COO-)一定大于c(Na+)与 c(NH4+)之和 | |
| B. | 常温下将0.01molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液.溶液中n(CH3COO-)+n(OH-)-n(H+)=0.006mol | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)<c(NO3-) | |
| D. | 物质的量浓度相等的NaF和NaCN溶液中阴离子总数相等 |
(1)向FeBr2溶液中滴加少量氯水,溶液变黄.你认为使溶液变黄的微粒其符号是Fe3+
用实验证明你的观点,简述实验操作及现象取适量反应后的溶液滴加KSCN溶液变红
(2)用惰性电极电解由等物质的量的NaBr,KI,NaCl组成的混合溶液,阳极首先发生的电极反应式是2I--2e-=I2
(3)己知常温下一些电解质的相关数据见表:
| H2CO3 | K${\;}_{{\;}_{{a}_{1}}}$=4.3×10-7 | HClO | Ka=2.95×10-8 |
| K${\;}_{{a}_{2}}$=5.61×10-11 | AgCl | Ksp=1.77×10-10 | |
| CH3COOH | Ka=1.76×10-5 | Ag2CrO4 | Ksp=1.12×10-12 |
②向浓度均为0.010mot•L一1的NaCl,Na2Cr04组成的混合溶液中逐滴加入浓度为
0,.010mol•L -1AgN03溶液,首先生成的沉淀其化学式为AgCl.
(4)分别向四份各100ML,浓度均为2mo1•L-1的FeC13溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | |
| FeCl3溶液体积/mL | 100 | 100 | 100 | 100 |
| 加入粉末质量/g | 3 | 6.6 | 9 | 12 |
| 剩余粉末质量/g | 0 | 0.64 | 3.2 | 6.4 |
②根据表中的数据分析I反应后的溶液中存在的金属阳离子有〔用离子符号表示)Fe3+、Fe2+、Cu2+.
| A. | 按系统命名法, 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 分子是为C5H12O且可与金属钠反应放出氢气的有机物有 (不考虑立体异构) 8种 | |
| D. | 某单炔烃,氢化后的产物结构简式为: ,则该烃可能有的结构有4种 ,则该烃可能有的结构有4种 |
| A. | 苯 | B. | 乙烯 | C. | 乙烷 | D. | 乙酸 |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | ||||
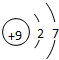 ;最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式)
;最高价氧化物对应的水化物中碱性最强的是NaOH(填化学式)(2)元素④和元素⑤相比较,气态氢化物稳定性较强的是H2O(填化学式),元素④氢化物的电子式是
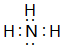 .
.(3)元素⑤与元素⑨相比较,非金属性较强的是氧(填名称),可以验证该结论的实验是(b)(填编号).
(a) 将它们的氢化物溶于水,测PH值,比较溶液的酸性
(b) 取它们的单质分别与氢气反应,比较同物质的量放出热量的多少
(c) 加热两种元素的氢化物,比较它们的熔沸点高低
(4)⑤和⑦按1:1形成的化合物的化学式Na2O2
(5)写出元素⑦和元素⑧的最高价氧化物的水化物相互反应的化学方程式:NaOH+Al(OH)3=NaAlO2+2H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
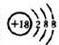 .
.(2)表中能形成两性氢氧化物的元素是Al (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O=2KAlO2+3H2↑.
(3)④元素与⑦元素形成的化合物的电子式
 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4.(填化学式)
| A. | 少量金属钠保存在煤油中 | |
| B. | 试剂瓶中的液溴可用水封存,防止溴挥发 | |
| C. | 保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉 | |
| D. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
 ;
; ;
; 和a个-CH3,其余为-OH,则-OH 的个数为m+2-a
和a个-CH3,其余为-OH,则-OH 的个数为m+2-a