题目内容
用盐酸测定碳酸钠时既可用酚酞作指示剂又可用甲基橙(一种酸碱指示剂)作指示剂,现分别用酚酞和甲基橙作指示剂,用0.1000mol/L的HCl滴定20.00mL的纯碱溶液,滴定终点时分别用去了20.00mL、40.00mL的盐酸,下列说法中不正确的是( )
| A、用酚酞作指示剂时滴定的总反应为:Na2CO3+HCl═NaHCO3+NaCl |
| B、用甲基橙作指示剂时滴定的总反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O |
| C、可用碱式滴定管量取所需要的Na2CO3溶液 |
| D、若酸式滴定管没有用标准溶液润洗,则所测得的碳酸钠溶液浓度偏低 |
考点:中和滴定
专题:实验题,实验评价题
分析:甲基橙和酚酞的变色范围分别约为pH在3-5和8-10,结合所用盐酸的体积分析,可知用酚酞作指示剂时反应为:Na2CO3+HCl═NaHCO3+NaCl,用甲基橙作指示剂时反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O;Na2CO3和NaHCO3溶液均显碱性,量取时使用碱式滴定管;据c(Na2CO3)=
中消耗标准液V(HCl)的大小判断误差.
| c(HCl)?V(HCl) |
| V(NaOH) |
解答:
解:A、酚酞的变色范围约为pH在8-10之间,结合所用盐酸的体积分析,可知用酚酞作指示剂时反应为:Na2CO3+HCl═NaHCO3+NaCl,故A正确;
B、甲基橙的变色范围约为pH在3-5之间,结合所用盐酸的体积分析,用甲基橙作指示剂时反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O,故B正确;
C、Na2CO3和NaHCO3溶液均显碱性,量取时使用碱式滴定管,故C正确;
D、c(Na2CO3)=
,酸式滴定管没有用标准溶液润洗,消耗标准液体积增大,导致所测得的碳酸钠溶液浓度偏高,故D错误;
故选D.
B、甲基橙的变色范围约为pH在3-5之间,结合所用盐酸的体积分析,用甲基橙作指示剂时反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O,故B正确;
C、Na2CO3和NaHCO3溶液均显碱性,量取时使用碱式滴定管,故C正确;
D、c(Na2CO3)=
| c(HCl)?V(HCl) |
| V(NaOH) |
故选D.
点评:本题考查了酸碱中和滴定中指示剂的选择对反应结果的影响以及误差分析,题目难度中等.

练习册系列答案
相关题目
等物质的量的CH4和NH3相比较,下列结论错误的是?( )
| A、它们的分子个数比为1:1 |
| B、它们的原子个数比为5:4 |
| C、它们的电子个数比为1:1 |
| D、它们的体积比为1:1 |
下列各组离子能在酸性的无色溶液中大量共存的是( )
| A、Na+、NH4+、Cl-、CO32- |
| B、Fe3+、Mg2+、SO42-、NO3- |
| C、Ba2+、Ca2+、Br-、SO42- |
| D、Zn2+、Ca2+、NO3-、Cl- |
下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A、NaCl晶体、BaSO4 |
| B、液态的醋酸、酒精 |
| C、铜、二氧化硫 |
| D、熔融的KNO3、硫酸溶液 |
某元素R的阴离子R2-核外共有a个电子,核内有b个中子,则下列表示R原子的符号中,正确的是( )
| A、abR |
| B、a+ba+2R |
| C、a+b-2a+2R |
| D、a+b-2a-2R |
下列离子方程式正确的是( )
| A、向硫酸铝铵溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-═AlO2-+2BaSO4↓+NH3?H2O+2H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O |
| C、在碳酸氢镁溶液中加入过量氢氧化钠溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| D、向NH4HCO3溶液中加过量的NaOH溶液并加热NH4++OH-═△NH3↑+H2O |
 有A、B、C、D、E五种元素,其相关信息如下:
有A、B、C、D、E五种元素,其相关信息如下: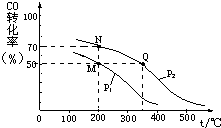 开发新能源和三废处理都是可持续发展的重要方面.CO在催化剂作用下可以与H2反应生成甲醇:
开发新能源和三废处理都是可持续发展的重要方面.CO在催化剂作用下可以与H2反应生成甲醇: