题目内容
PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A、10min内,v(Cl2)=0.04mol/(L?min) |
| B、当反应达到平衡时,容器中Cl2为1.2mol |
| C、升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)=0.2mol/L |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、由于平衡时生成PCl5的浓度为0.4mol/L,根据化学方程式可知,反应用掉Cl2的浓度为0.4mol/L,根据v=
计算反应速率;
B、由A的分析可知,平衡时容器中Cl2浓度为(1.0-0.4)mol/L,体积是2L,据此计算;
C、反应的平衡常数减小,则平衡逆向移动,PCl3的转化率变小,据此判断;
D、利用压强对平衡的影响判断.
| △c |
| t |
B、由A的分析可知,平衡时容器中Cl2浓度为(1.0-0.4)mol/L,体积是2L,据此计算;
C、反应的平衡常数减小,则平衡逆向移动,PCl3的转化率变小,据此判断;
D、利用压强对平衡的影响判断.
解答:
解:A、由于平衡时生成PCl5的浓度为0.4mol/L,根据化学方程式可知,反应用掉Cl2的浓度为0.4mol/L,根据v=
计算反应速率为
mol/(L?min)=0.04mol/(L?min),A正确;
B、由A的分析可知,平衡时容器中Cl2浓度为(1.0-0.4)mol/L=0.6mol/L,体积是2L,所以平衡时,容器中Cl2的物质的量为1.2mol,故B正确;
C、升高温度,反应的平衡常数减小,则平衡逆向移动,PCl3的转化率变小,故C错误;
D、平衡后移走2.0mol PCl3和1.0mol Cl2,相当于起始量为原来的一半,如果平衡不移动,则c(PCl5)=0.2mol/L,由于容器体积不变,所以压强减小,而该反应是气体体积减小的反应,减压平衡逆向移动,所以c(PCl5)<0.2mol/L,故D错误;
故选CD.
| △c |
| t |
| 0.4 |
| 10 |
B、由A的分析可知,平衡时容器中Cl2浓度为(1.0-0.4)mol/L=0.6mol/L,体积是2L,所以平衡时,容器中Cl2的物质的量为1.2mol,故B正确;
C、升高温度,反应的平衡常数减小,则平衡逆向移动,PCl3的转化率变小,故C错误;
D、平衡后移走2.0mol PCl3和1.0mol Cl2,相当于起始量为原来的一半,如果平衡不移动,则c(PCl5)=0.2mol/L,由于容器体积不变,所以压强减小,而该反应是气体体积减小的反应,减压平衡逆向移动,所以c(PCl5)<0.2mol/L,故D错误;
故选CD.
点评:本题主要考查了化学反应速率的计算、平衡移动中有关物理量的变化,中等难度,解题时注意基础知识的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、MgCO3易溶于水 |
| B、硅单质常用作半导体材料、光导纤维和太阳能电池 |
| C、铜与硫在加热条件下生成Cu2S |
| D、Na2SiO3溶液通常保存在带玻璃塞的磨口试剂瓶中 |
生产铅蓄电池时,在两极板上的铅、锑合金棚架上均匀涂上膏状的PbSO4,干燥后再安装,充电后即可使用,发生的反应是:
PbO2+Pb+2H2SO4
2PbSO4+2H2O,下列对铅蓄电池的说法错误的是( )
PbO2+Pb+2H2SO4
| 放电 |
| 充电 |
| A、需要定期补充硫酸 | ||
| B、放电时电解质的密度减小 | ||
| C、放电时铅是负极,PbO2是正极 | ||
D、放电时负极上发生的反应是Pb+S
|
下列实验装置图正确的是( )
A、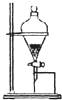 分力乙醇和乙醛 |
B、 实验室制氨气 |
C、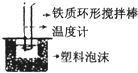 反应热的测定 |
D、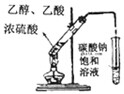 实验室制乙酸乙酯 |
下列各组物质中属于同分异构体的是( )
| A、金刚石和C60 |
B、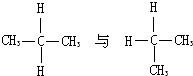 |
C、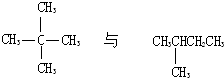 |
| D、CH4与CH3CH3 |
在温度、容积相同的 3 个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
(已知N2(g)+3H2 (g)?2NH3(g)△H=-92.4kJ?mol-1)
下列说法不正确的是( )
(已知N2(g)+3H2 (g)?2NH3(g)△H=-92.4kJ?mol-1)
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3 的浓度(mol?L-1 ) | c1 | c2 | c3 |
| 反应的能量变化 | 放出 akJ | 吸收 bkJ | 吸收 ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、2p2>p3 |
| B、a+b=92.4 |
| C、2c1>c3 |
| D、α1+α2=1 |
室温时,浓度都为0.1mol/L的HA、HC、HD三种一元酸溶液,其中HA溶液中c(H+)=0.01mol/L,HC的pH值为3,HD溶液中c(OH-)=10-13mol/L,则三种酸对应的钠盐在物质的量浓度和温度相同的条件下,溶液的pH值由大到小的顺序为( )
| A、NaA>NaC>NaD |
| B、NaC>NaA>NaD |
| C、NaD>NaA>NaC |
| D、NaC>NaD>NaA |