题目内容
用黄铁矿可以制取H2SO4,再用H2SO4可以制取化肥(NH4)2SO4.煅烧含FeS280.2%的黄铁矿75.0t,最终生产出79.2t(NH4)2SO4.已知NH3的利用率为92.6%,H2SO4的利用率为89.8%,试求黄铁矿制取H2SO4时的损失率为( )
| A、23.8% |
| B、33.4% |
| C、35.6% |
| D、63.8% |
考点:化学方程式的有关计算
专题:计算题
分析:根据S原子守恒可得FeS2与(NH4)2SO4的关系:FeS2~2H2SO4~2(NH4)2SO4,硫酸的利用率可归为FeS2的利用率,结合关系式计算.
解答:
首先须搞清 H2SO4的利用率与 FeS2利用率的关系.并排除 NH3利用率的干扰作用.
解:设黄铁矿转化为硫酸的利用率为x,则:
FeS2~2 H2SO4~2 (NH4)2SO4
120 264
75.0 t×80.2%×89.8%?x 79.2 t
故120:264=(75.0 t×80.2%×89.8%?x):79.2 t
解得x=66.65%
黄铁矿的损失率为:1-66.65%=33.35%,
故选B.
解:设黄铁矿转化为硫酸的利用率为x,则:
FeS2~2 H2SO4~2 (NH4)2SO4
120 264
75.0 t×80.2%×89.8%?x 79.2 t
故120:264=(75.0 t×80.2%×89.8%?x):79.2 t
解得x=66.65%
黄铁矿的损失率为:1-66.65%=33.35%,
故选B.
点评:本题考查化学方程式计算,注意利用关系式进行计算,关键理解中间产物的损耗量(或转化率、利用率)都可归为起始原料的损耗量(或转化率、利用率),元素的损失率等于该化合物的损失率,难度中等.

练习册系列答案
相关题目
下列有关说法正确的是( )
A、以下是精确配制一定物质的量浓度NaOH溶液的实验步骤,其中操作正确的有4步 |
| B、苯的硝化实验三种溶液混合过程中,应先在试管中加入浓硝酸,再沿试管壁缓慢加入浓硫酸混合均匀,冷却到50℃以下,再在不断振荡下逐滴加入苯 |
| C、火柴头中硫元素的检测实验中,应用少量1mol?L-1较大浓度的高锰酸钾溶液来吸收SO2气体,以便于观察到褪色的明显实验现象 |
| D、在试管中加入2mL硝酸银溶液,然后加入几滴NaCl溶液,再加入几滴KI溶液,可以观察到白色沉淀变成黄色沉淀,可以说明AgI的KSP小于AgCl的KSP |
 一定条件下,在绝热恒容2L密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)+Q,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )
一定条件下,在绝热恒容2L密闭容器中进行反应:N2(g)+3H2(g)?2NH3(g)+Q,若反应过程中n(H2)和n(NH3)随时间变化的关系如图所示,则下列有关叙述中一定正确的是( )| A、若在t2时刻再充入一定量He,达平衡时C(H2)<0.4mol/L |
| B、a点表示NH3生成速率与NH3分解速率相等 |
| C、b点和c点H2的转化率相等 |
| D、若在t1时刻再充入一定量H2,达平衡时化学平衡常数变小 |
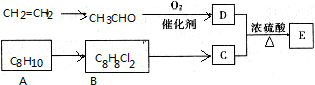
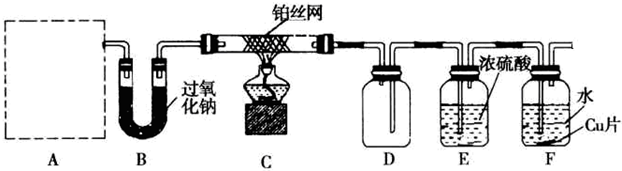
 B.
B. C.
C. D.
D.