题目内容
19.常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是( )| A. |  | B. |  | C. | 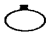 | D. |  |
分析 等质量的CH4、CO2、O2、SO2四种气体的物质的量与其摩尔质量成反比,即摩尔质量越大,则物质的量越小,在同温同压下,体积越小,据此进行解答.
解答 解:气体的物质的量n=$\frac{m}{M}$,在同温同压下,气体摩尔体积相同,气体的体积V=n•Vm,即V=$\frac{m}{M}$Vm可知,摩尔质量越大,体积越小,
CH4、CO2、O2、SO2的摩尔质量分别为16g/mol、44g/mol、32g/mol、64g/mol,SO2的摩尔质量最大,故体积最小,故A正确,
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积、摩尔质量之间关系即可解答,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
9.我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与氧化铁发生铝热反应进行焊接而成的.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )
| A. | Fe元素的化合价升高 | B. | Al化合价升高 | ||
| C. | 该反应是化合反应 | D. | Al化合价没变 |
10.下列叙述正确的是( )
| A. | 碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 | |
| B. | 石英、水晶、硅石的主要成分都是二氧化硅 | |
| C. | 二氧化硅的化学性质活泼,能与任意的酸、碱发生反应 | |
| D. | 碳族元素的单质都有导电性 |
7.在1gO2和1gO3中( )
| A. | 所含原子数不相同 | B. | 所含分子数相同 | ||
| C. | 物质的量相同 | D. | 所含质子数相同 |
14.肼(N2H4)是一种高能燃料,常温下是液体,燃烧产生巨大能量,可作为航天火箭的推动力.下列叙述中正确的是( )
| A. | N2H4的摩尔质量为32 | |
| B. | 1 molN2H4的质量为32 g•mol-1 | |
| C. | 在标准状况下,1 mol N2H4的体积约为22.4L | |
| D. | 6.02×1023个N2H4分子的质量为32g |
4.1.42g R元素可与氧元素组成2.38g氧化物X,或组成3.66g氧化物Y,则X、Y的化学式可能是( )
| A. | R2O和R2O5 | B. | R2O3和R2O5 | C. | R2O3和R2O7 | D. | R2O和R2O3 |
11.燃烧由CH4和C3H8组成的混合气体,生成3.52gCO2和1.98gH2O.此混合气体中CH4与C3H8的体积比为( )
| A. | 1:5 | B. | 1:2 | C. | 3:2 | D. | 2:1 |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1 KSCN溶液中:Fe3+、NH4+、Br-、SO42- | |
| B. | $\frac{{c(O{H^-})}}{{c({H^+})}}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 0.1 mol•L-1 Ca(NO3)2溶液中:Na+、NH4+、CO32-、CH3COO- |
9.下列指定溶液中,一定能够大量共存的离子组是( )
| A. | 由水电离产生的两种离子浓度关系为c(H+)•c(OH-)=10-24的溶液中:Al3+、Na+、Cl-、SO42- | |
| B. | 含有大量AlO2-的溶液中:HCO3-、K+、Cl-、NO3- | |
| C. | 常温下,PH=7的溶液中:Fe3+、Na+、NO3-、SO42- | |
| D. | 能使广泛PH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- |