题目内容
S元素最可能是( )
| A、s区元素 | B、p区元素 |
| C、d区元素 | D、稀有气体元素 |
考点:元素周期表的结构及其应用
专题:
分析:S的原子序数为16,电子排布为1s22s22p63s23p4,最后填充的电子为p电子,以此来解答.
解答:
解:S的原子序数为16,电子排布为1s22s22p63s23p4,最后填充的电子为p电子,则S元素为p区元素,
故选B.
故选B.
点评:本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、电子排布为解答的关键,注意利用最后填充的电子判断元素的分区,题目难度不大.

练习册系列答案
相关题目
四位同学根据离子方程式:Zn+Cu2+=Zn2++Cu设计原电池,其设计如表所示,其不正确的是( )
| A | B | C | D | |
| 正极 | Cu | Ag | 石墨 | Mg |
| 负极 | Zn | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | CuSO4 | CuCl2 | Cu(NO3)2 |
| A、A | B、B | C、C | D、D |
 已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑硝基与氢氧化钠的反应),则a是( )
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如图:1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑硝基与氢氧化钠的反应),则a是( )| A、5mol | B、6mol |
| C、7mol | D、8mol |
已知X、Y、Z为三种原子序数相连的元素,最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4.则下列说法正确的是( )
| A、气态氢化物的稳定性:HX>H2Y>ZH3 |
| B、非金属性:Y<X<Z |
| C、原子半径:X>Y>Z |
| D、原子序数:Z>Y>X |
已知17X、34Y、35Z三种原子,据其在周期表中的位置,判断下列说法正确的是( )
| A、原子半径:X>Y>Z |
| B、气态氢化物的稳定性Y>X>Z |
| C、单质熔点:Y>X>Z |
| D、简单阴离子的还原性:Y>Z>X |
大理石是一种重要的化工原料,其主要成分可以反应生成一系列物质,如下图所示.
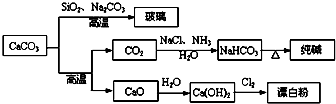
下列说法正确的是( )

下列说法正确的是( )
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、向饱和碳酸钠溶液中通入过量CO2,溶液变浑浊 | ||||
| D、制取玻璃和漂白粉所涉及的反应都是非氧化还原反应 |
下列物质中含有非极性共价键的离子化合物是( )
| A、Ba(OH)2 |
| B、CaCl2 |
| C、H2O |
| D、Na2O2 |
 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.