题目内容
某温度下,将Cl2通入NaOH 溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-、ClO3-的浓度之比为1:1,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为( )
| A、2:1 | B、1:2 |
| C、3:1 | D、4:1 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:Cl2生成ClO-与ClO3-是被氧化的过程,Cl2生成NaCl是被还原的过程,氧化还原反应中氧化剂和还原剂之间得失电子数目相等,根据ClO-与ClO3-的物质的量浓度之比可计算失去电子的总物质的量,进而可计算得到电子的总物质的量,可计算被还原的氯元素的物质的量,则可计算被还原的氯元素和被氧化的氯元素的物质的量之比.
解答:
解:Cl2生成ClO-与ClO3-是被氧化的过程,化合价分别由0价升高为+1价和+5价,
ClO-与ClO3-的物质的量浓度之比为1:1,
则可设ClO-为1mol,ClO3-为1mol,被氧化的Cl共为2mol,
失去电子的总物质的量为1mol×(1-0)+1mol×(5-0)=6mol,
氧化还原反应中氧化剂和还原剂之间得失电子数目相等,
Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,
则得到电子的物质的量也应为6mol,
则被还原的Cl的物质的量为6mol,
所以被还原的氯元素和被氧化的氯元素的物质的量之比为6mol:2mol=3:1,
故选C.
ClO-与ClO3-的物质的量浓度之比为1:1,
则可设ClO-为1mol,ClO3-为1mol,被氧化的Cl共为2mol,
失去电子的总物质的量为1mol×(1-0)+1mol×(5-0)=6mol,
氧化还原反应中氧化剂和还原剂之间得失电子数目相等,
Cl2生成KCl是被还原的过程,化合价由0价降低为-1价,
则得到电子的物质的量也应为6mol,
则被还原的Cl的物质的量为6mol,
所以被还原的氯元素和被氧化的氯元素的物质的量之比为6mol:2mol=3:1,
故选C.
点评:本题考查氧化还原反应的计算,题目难度不大,本题注意从氧化还原反应中氧化剂和还原剂之间得失电子数目相等的角度计算,注意守恒法的利用.

练习册系列答案
相关题目
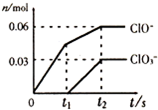 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示.下列说法不正确的是( )| A、苛性钾溶液中KOH的质量是16.8g |
| B、氯气在反应中既是氧化剂也是还原剂 |
| C、最终消耗氯气的物质的量为0.09mol |
| D、ClO3-的生成是由于温度升高引起的 |
X、Y、Z三种元素在周期表中,X、Y同主族,Y和Z同周期,它们的原子的最外层电子数之和为16,则这三种元素可能是( )
| A、Na、K、Ca |
| B、N、P、S |
| C、F、Cl、S |
| D、O、S、Cl |
常温常压下,用等质量的CH4、CO2、O2、SO2分别吹出如图四个气球,其中气体为CH4的是( ) 

| A、图中A为CH4、B为CO2 |
| B、图中A为SO2、C为O2 |
| C、图中B为CO2、D为CH4 |
| D、图中C为CH4、D为O2 |
某元素气态氢化物的化学式为XH3,则此元素最高价氧化物对应的水化物的化学式应是( )
| A、HXO4 |
| B、H2XO3 |
| C、H2XO4 |
| D、H3XO4 |
化学与科技、社会、生活有着密切的联系,下列有关说法正确的是( )
| A、乙醇汽油可用普通汽油与燃料乙醇调和而成.乙醇和汽油都是可再生能源,应大力推广乙醇汽油 |
| B、区分蛋白质胶体和葡萄糖溶液可利用丁达尔效应 |
| C、奥运场馆鸟巢使用了钒氮合金高新钢,这种新型钢材的熔点、硬度均比纯铁高 |
| D、可吸入颗粒物中含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |
某元素原子价电子构型3d104S2,其应在( )
| A、第四周期ⅡA族 |
| B、第四周期ⅡB族 |
| C、第四周期ⅦA族 |
| D、第四周期ⅦB族 |