题目内容
18.依据元素周期表及元素周期律,下列推断正确的是( )| A. | H2SiO3的酸性比H2CO3的强 | |
| B. | Mg(OH)2的碱性比Be(OH)2的强 | |
| C. | HF、HCl、HBr、HI的热稳定性依次增强 | |
| D. | 若M+和R2-的核外电子层结构相同,则原子序数:R>M |
分析 A、同主族元素,从上到下,最高价含氧酸的酸性逐渐减弱;
B、同周期,从左到右,最高价氧化物对应水化物的碱性减弱;
C、同主族元素,从上到下,氢化物的稳定性性逐渐减弱;
D、电子层一样,阳离子的原子序数更大.
解答 解:A、同主族元素,从上到下,最高价含氧酸的酸性逐渐减弱,H2SiO3的酸性比H2CO3的弱,故A错误;
B、同主族元素,从上到下,最高价氧化物对应水化物的碱性增强,Mg(OH)2的碱性比Be(OH)2的强,故B正确;
C、同主族元素,从上到下,氢化物的稳定性性逐渐减弱,HF、HCl、HBr、HI的热稳定性依次减弱,故C错误;
D、根据电子层一样,阳离子的原子序数更大,M+和R2-的核外电子层结构相同,则原子序数:R<M,故D错误.
故选B.
点评 本题考查学生元素周期表和元素周期律的应用知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.0.02mol•L-1的HCN溶液与0.02mol•L-1的NaCN溶液等体积混合,已知混合液中c(CN-)<c(Na+),则下列关系不正确的是( )
| A. | c(HCN)+c(CN-)=0.02 mol•L-1 | B. | c(Na+)>c(OH-)>c (CN-)>c(H+) | ||
| C. | c(Na+)+c(H+)=c(CN-)+c(OH-) | D. | c(HCN)>c(CN-) |
6. (1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
依据表中的数据,总结烯类化合物与溴发生加成反应时,反应速率与C=C上取代基的种类、个数的关系①C=C上的H被甲基(烷基)取代,有利于加成反应、②甲基(烷基)越多,速率越大、③C=C上的H被Br(卤素)取代,不利于加成反应.
(2)下列化合物与HCl加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D(填代号).
A.(CH3)2C=C(CH3)2B.CH3CH=CHCH3C.CH2=CH2D.CH2=CHCl
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2CH2Br(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3(主要产物)+CH3CH2CH2CH2OH(次要产物)
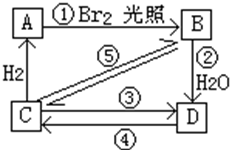
在下图中B、C、D都是相关反应中的主要产物(部分反应条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、9个氢原子.图框中B的结构简式为(CH3)3CBr;属于取代反应的有①②(填框图中的序号,下同),属于消去反应的有③;写出反应④的化学方程式(只写主要产物,表明反应条件):(CH3)3C-OH $→_{△}^{浓硫酸}$CH2=C(CH3)2+H2O.
 (1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
(2)下列化合物与HCl加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是D(填代号).
A.(CH3)2C=C(CH3)2B.CH3CH=CHCH3C.CH2=CH2D.CH2=CHCl
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2CH2Br(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3(主要产物)+CH3CH2CH2CH2OH(次要产物)
在下图中B、C、D都是相关反应中的主要产物(部分反应条件、试剂被省略),且化合物B中仅有4个碳原子、1个溴原子、9个氢原子.图框中B的结构简式为(CH3)3CBr;属于取代反应的有①②(填框图中的序号,下同),属于消去反应的有③;写出反应④的化学方程式(只写主要产物,表明反应条件):(CH3)3C-OH $→_{△}^{浓硫酸}$CH2=C(CH3)2+H2O.
13.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 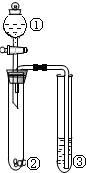 |
| A | 稀盐酸 | 石灰石 | 稀的碳酸钠溶液 | 溶解度:碳酸钠>碳酸氢钠 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸有脱水性、强氧化性 | |
| C | 浓硫酸 | Na2SO3 | 品红溶液 | 浓硫酸具有强氧化性 | |
| D | 浓盐酸 | Na2CO3 | Na2SiO3溶液 | 酸性:盐酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
10.向21.6g Fe3O4、Fe2O3、FeO、Cu的混合物中加入0.5mol•L-1的硫酸溶液420mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A. | 1.12 g | B. | 2.24 g | C. | 3.36 g | D. | 6.40 g |
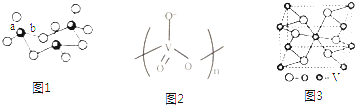
 ,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
,B最外层电子数是2,C的气态氢化物的水溶液呈碱性,据此填空:
 Al(OH)3
Al(OH)3 AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.
AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.