题目内容
7.下列说法中正确的一组是( )| A. | H2和D2互为同位素 | B. | 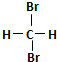 和 和 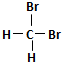 互为同分异构体 互为同分异构体 | ||
| C. | 正丁烷和异丁烷是同系物 | D. | 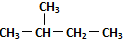 和 和 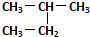 是同一种物质 是同一种物质 |
分析 A、同种元素的不同种原子间互为同位素
B、分子式相同而结构不同的化合物互为同分异构体;
C、结构相似,分子组成上相差一个或若干个CH2原子团的化合物互为同系物;
D、结构相同,分子式也相同的物质为同一种物质.
解答 解:A、同种元素的不同种原子间互为同位素,而H2和D2不是原子而是单质,故不是同位素,故A错误;
B、分子式相同而结构不同的化合物互为同分异构体,而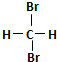 和
和 的分子组成和结构均相同,故是同一种物质而不是同分异构体,故B错误;
的分子组成和结构均相同,故是同一种物质而不是同分异构体,故B错误;
C、结构相似,分子组成上相差一个或若干个CH2原子团的化合物互为同系物,而正丁烷和异丁烷的分子式相同而结构不同,故不是同系物,故C错误;
D、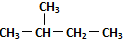 和
和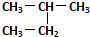 的结构相同,分子式也相同,故为同一种物质,故D正确.
的结构相同,分子式也相同,故为同一种物质,故D正确.
故选D.
点评 本题考查了四同概念的辨析,难度不大,掌握概念的要点是关键,应注意的是互为同系物的化合物的分子式必须不同.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
18.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 1NA个氢气分子所占的体积为22.4 L | |
| B. | 2NA个二氧化碳分子的质量为88 g | |
| C. | 0.1 mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| D. | 17 g NH3中所含原子数为NA |
15.下列实验方案合理的是( )
| A. | 配制银氨溶液:在一定量氨水溶液中,滴加AgNO3至沉淀恰好溶解 | |
| B. | 配制Cu(OH)2悬浊液:在一定量CuSO4溶液中,加入少量NaOH溶液 | |
| C. | 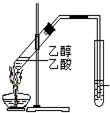 制备乙酸乙酯:用如图所示的实验装置 制备乙酸乙酯:用如图所示的实验装置 | |
| D. | 鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中 |
2.在一定温度下,某体积不变的密闭容器中,反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A. | 混合气体的密度不变 | |
| B. | 容器内的总压强不随时间变化 | |
| C. | 容器中各组分的体积分数不随时间变化 | |
| D. | 单位时间内生成2n mol的AB,同时生成n mol的B2 |
12.下列关于苯的结构和性质说法,正确的是( )
| A. | 苯是无色无味的液态径,不易燃烧 | |
| B. | 苯与浓硝酸、浓硫酸混合共热可制取硝基苯 | |
| C. | 溴水能与苯发生加成反应而褪色 | |
| D. | 在一定条件下苯与氢气反应制取环己烷,说明苯分子结构中有碳碳双键 |
19.(Se)是人体必需的一种微量元素,其单质可用于制光敏电阻、复印机的硒鼓等等.工业上提取硒的方法之一是用硫酸和硝酸钠处理含硒的工业废料,得到亚硒酸(H2SeO3)和少量硒酸(H2SeO4),富集后再将它们与盐酸共热,将H2SeO4转化为H2SeO3,主要反应为2HCl+H2SeO4═H2SeO3+H2O+Cl2↑,然后向溶液中通入SO2将硒元素还原为单质硒沉淀.据此正确的判断为( )
| A. | H2SeO4的氧化性比Cl2弱 | B. | SeO2的氧化性比SO2弱 | ||
| C. | H2SeO4的氧化性比H2SeO3强 | D. | 浓H2SeO4的氧化性比HNO3强 |
20.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了十种元素在周期表中的位置,用化学用语回答下列问题:
请回答:(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)形成化合物种类最多的元素是C(填元素符号),其稳定氧化物的结构式为O=C=O.
(3)⑤、⑥、⑦、⑧四种元素所对应的气态氢化物最稳定的是H2O,最不稳定的是SiH4(均填化学式).
(4)以上第三周期元素中的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式),二者发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(5)①、②、③的原子半径由大到小的顺序为K>Na>Mg(填元素符号).
(6)⑦元素的氢化物在常温下与①发生反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
(7)③、④两元素相比较,金属性较强的是Mg(填元素符号),可以验证该结论的方法有ACD(填编号).
A.将这两种元素的块状单质分别放入热水中看与水反应的剧烈程度
B.比较二者与某非金属反应时失电子数目多少
C.比较二者的最高价氧化物的水化物碱性强弱
D.看形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应的剧烈程度.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑦ | ||||||
| 3 | ① | ③ | ④ | ⑥ | ⑧ | ⑨ | ⑩ | |
| 4 | ② |
 .
.(2)形成化合物种类最多的元素是C(填元素符号),其稳定氧化物的结构式为O=C=O.
(3)⑤、⑥、⑦、⑧四种元素所对应的气态氢化物最稳定的是H2O,最不稳定的是SiH4(均填化学式).
(4)以上第三周期元素中的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式),呈两性的是Al(OH)3(填化学式),二者发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(5)①、②、③的原子半径由大到小的顺序为K>Na>Mg(填元素符号).
(6)⑦元素的氢化物在常温下与①发生反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
(7)③、④两元素相比较,金属性较强的是Mg(填元素符号),可以验证该结论的方法有ACD(填编号).
A.将这两种元素的块状单质分别放入热水中看与水反应的剧烈程度
B.比较二者与某非金属反应时失电子数目多少
C.比较二者的最高价氧化物的水化物碱性强弱
D.看形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应的剧烈程度.
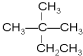 ④癸烷 ⑤CH3COOH
④癸烷 ⑤CH3COOH  ⑦
⑦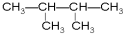 ⑧
⑧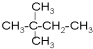 ⑨丙烷
⑨丙烷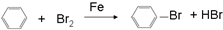 ;
; ;
; .
.