题目内容
碳及其化合物与人类生产、生活密切相关.请回答下列问题:
(1)在化工生产过程中,少量CO的存在会引起催化剂中毒.为了防止催化剂中毒,常用SO2将CO氧化,SO2被还原为S.
已知:C(s)+
O2(g)═CO(g)△H1=-126.4kJ/mol
C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
S(s)+O2(g)═SO2(g)△H3=-296.8kJ?mol-1
则SO2氧化CO的热化学反应方程式:
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).
①CO在不同温度下的平衡转化率与压强的关系如图1所示,该反应△H 0(填“>”或“<”).
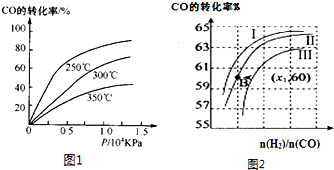
图2表示CO的转化率与起始投料比[
]、温度的变化关系,
曲线I、Ⅱ、Ⅲ对应的平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为 ;测得B(X,60)点氢气的转化率为40%,则x1= .
②在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是 (填序号).
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度增大
③一定条件下,将2mol CO和2mol H2置于容积为2L固定的密闭容器中发生上述反应,反应达到平衡时CO与H2体积之比为2:1,则平衡常数K= .
(3)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水.
原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,
总反应为:2CH3CHO+H2O?CH3CHOH+CH3CHOOH.
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示:
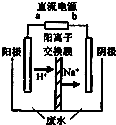
①电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体,阳极电极反应分别为:
4OH--4e-═O2↑+2H2O; .
②在实际工艺处理过程中,阴极区乙醛的去除率可达60%.若在两极区分别注入1m3乙醛的含量为300mg/L的废水,可得到乙醇 kg(计算结果保留2位小数)
(1)在化工生产过程中,少量CO的存在会引起催化剂中毒.为了防止催化剂中毒,常用SO2将CO氧化,SO2被还原为S.
已知:C(s)+
| 1 |
| 2 |
C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
S(s)+O2(g)═SO2(g)△H3=-296.8kJ?mol-1
则SO2氧化CO的热化学反应方程式:
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).
①CO在不同温度下的平衡转化率与压强的关系如图1所示,该反应△H

图2表示CO的转化率与起始投料比[
| n(H2) |
| n(CO) |
曲线I、Ⅱ、Ⅲ对应的平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为
②在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度增大
③一定条件下,将2mol CO和2mol H2置于容积为2L固定的密闭容器中发生上述反应,反应达到平衡时CO与H2体积之比为2:1,则平衡常数K=
(3)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水.
原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,
总反应为:2CH3CHO+H2O?CH3CHOH+CH3CHOOH.
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示:

①电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体,阳极电极反应分别为:
4OH--4e-═O2↑+2H2O;
②在实际工艺处理过程中,阴极区乙醛的去除率可达60%.若在两极区分别注入1m3乙醛的含量为300mg/L的废水,可得到乙醇
考点:热化学方程式,化学平衡常数的含义,化学平衡的影响因素,转化率随温度、压强的变化曲线,电解原理
专题:基本概念与基本理论
分析:(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)①依据定一议二的方法分析图象变化,温度越高,一氧化碳转化率越小,升温平衡逆向进行;设起始量氢气为x,一氧化碳物质的量为y,依据转化率分析计算;
②当正逆反应速率不相等时,化学平衡会向着正方向或是逆方向进行;
③依据平衡三段式列式计算平衡浓度,结合平衡常数概念计算;
(3)①阳极上失电子发生氧化反应,阴极上得电子发生还原反应;
②先根据废水的质量、乙醛的去除率计算去除乙醛的质量,再根据乙醛和乙醇的关系式计算生成乙醇的质量.
(2)①依据定一议二的方法分析图象变化,温度越高,一氧化碳转化率越小,升温平衡逆向进行;设起始量氢气为x,一氧化碳物质的量为y,依据转化率分析计算;
②当正逆反应速率不相等时,化学平衡会向着正方向或是逆方向进行;
③依据平衡三段式列式计算平衡浓度,结合平衡常数概念计算;
(3)①阳极上失电子发生氧化反应,阴极上得电子发生还原反应;
②先根据废水的质量、乙醛的去除率计算去除乙醛的质量,再根据乙醛和乙醇的关系式计算生成乙醇的质量.
解答:
解:(1)已知:①C(s)+
O2(g)═CO(g)△H1=-126.4kJ/mol
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
③S(s)+O2(g)═SO2(g)△H3=-296.8kJ?mol-1
依据盖斯定律计算②×2-①×2-③得到SO2氧化CO的热化学反应方程式:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-237.4kJ?mol-1;
故答案为:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-237.4kJ?mol-1;
(2)①依据定一议二的方法分析图象变化,温度越高,一氧化碳转化率越小,升温平衡逆向进行,逆向是吸热反应,正反应为放热反应,△H<0,温度越高平衡逆向进行,平衡常数减小,所以 K1>K2>K3,设起始量氢气为x,一氧化碳物质的量为y;
CO(g)+2H2(g)?CH3OH(g)
y x 0
0.6y 0.4x
则0.6y:0.4x=1:2
x:y=3
故答案为:<; K1>K2>K3;3;
②化学平衡的标志是正逆反应速率相等,当逆反应速率大于正反应速率时,说明反应是逆向进行的,CO(g)+2H2(g)?CH3OH(g)△H<0;
A.正反应速率先增大后减小,说明反应正向进行,故A正确;
B.逆反应速率先增大后减小,说明反应逆向进行,故B错误;
C.化学平衡常数K值增大,说明平衡正向进行,故C正确;
D.反应物的体积百分含量增大,可能逆向进行,也可能正向进行,不能说明反应正向进行,故D错误;
E.恒容容器中加入生成物,平衡逆向进行,气体质量增大,条件不变,混合气体的密度增大,故E错误;
故答案为:AC;
③一定条件下,将2mol CO和2mol H2置于容积为2L固定的密闭容器中发生上述反应,反应达到平衡时CO与H2体积之比为2:1,设消耗一氧化碳浓度为x,
则 CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L) 1 1 0
变化量(mol/L) x 2x x
平衡量(mol/L)1-x 1-2x x
(1-x):(1-2x)=2:1
x=
则平衡常数K=
=4.5 L2?mol-2;
故答案为:4.5 L2?mol-2;
(3)①电解过程中,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,所以阳极上乙醛和氢氧根离子放电,所以除了氢氧根离子失电子外,乙醛失电子发生氧化反应,电极反应式为CH3CHO-2e-+H2O=CH3COOH+2H+;阴极上得电子,得电子的微粒有氢离子和乙醛,氢离子得电子生成氢气,电极反应式为4H++4e-=2H2↑,
故答案为:CH3CHO-2e-+H2O=CH3COOH+2H+;
②设生成乙醇的质量是x,
废水中乙醛的质量为1m3×0.3Kg/m3=0.3Kg,乙醛的去除率为60%,则反应的乙醛为0.18Kg,
CH3CHO+2e-+2H2O═CH3CH2OH+2OH-
44 46
0.18kg x
x=0.19kg
故答案为:0.19.
| 1 |
| 2 |
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
③S(s)+O2(g)═SO2(g)△H3=-296.8kJ?mol-1
依据盖斯定律计算②×2-①×2-③得到SO2氧化CO的热化学反应方程式:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-237.4kJ?mol-1;
故答案为:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-237.4kJ?mol-1;
(2)①依据定一议二的方法分析图象变化,温度越高,一氧化碳转化率越小,升温平衡逆向进行,逆向是吸热反应,正反应为放热反应,△H<0,温度越高平衡逆向进行,平衡常数减小,所以 K1>K2>K3,设起始量氢气为x,一氧化碳物质的量为y;
CO(g)+2H2(g)?CH3OH(g)
y x 0
0.6y 0.4x
则0.6y:0.4x=1:2
x:y=3
故答案为:<; K1>K2>K3;3;
②化学平衡的标志是正逆反应速率相等,当逆反应速率大于正反应速率时,说明反应是逆向进行的,CO(g)+2H2(g)?CH3OH(g)△H<0;
A.正反应速率先增大后减小,说明反应正向进行,故A正确;
B.逆反应速率先增大后减小,说明反应逆向进行,故B错误;
C.化学平衡常数K值增大,说明平衡正向进行,故C正确;
D.反应物的体积百分含量增大,可能逆向进行,也可能正向进行,不能说明反应正向进行,故D错误;
E.恒容容器中加入生成物,平衡逆向进行,气体质量增大,条件不变,混合气体的密度增大,故E错误;
故答案为:AC;
③一定条件下,将2mol CO和2mol H2置于容积为2L固定的密闭容器中发生上述反应,反应达到平衡时CO与H2体积之比为2:1,设消耗一氧化碳浓度为x,
则 CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L) 1 1 0
变化量(mol/L) x 2x x
平衡量(mol/L)1-x 1-2x x
(1-x):(1-2x)=2:1
x=
| 1 |
| 3 |
则平衡常数K=
| ||||
(1-
|
故答案为:4.5 L2?mol-2;
(3)①电解过程中,阳极上失电子发生氧化反应,阴极上得电子发生还原反应,所以阳极上乙醛和氢氧根离子放电,所以除了氢氧根离子失电子外,乙醛失电子发生氧化反应,电极反应式为CH3CHO-2e-+H2O=CH3COOH+2H+;阴极上得电子,得电子的微粒有氢离子和乙醛,氢离子得电子生成氢气,电极反应式为4H++4e-=2H2↑,
故答案为:CH3CHO-2e-+H2O=CH3COOH+2H+;
②设生成乙醇的质量是x,
废水中乙醛的质量为1m3×0.3Kg/m3=0.3Kg,乙醛的去除率为60%,则反应的乙醛为0.18Kg,
CH3CHO+2e-+2H2O═CH3CH2OH+2OH-
44 46
0.18kg x
x=0.19kg
故答案为:0.19.
点评:本题考查了热化学方程式书写和盖斯定律计算应用,化学平衡、平衡常数计算影响因素分析判断,图象分析理解应用,难度不大,注意燃料电池电极反应式的书写要结合电解质溶液.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法不正确的是( )
| A、放热反应不需加热即可发生 |
| B、化学反应均伴随有能量变化,这种能量变化除热能外,还可以是光能、电能等 |
| C、可燃物的燃烧热的大小与参与反应的可燃物的多少无关 |
| D、化学反应热效应数值与参与反应的物质多少有关 |
下列说法正确的是( )
| A、在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
| B、为降低铜锌原电池中的极化作用,可在电解质溶液中加入少量双氧水 |
| C、在制备硝酸钾晶体的实验中,趁热过滤时,承接滤液的小烧杯中先加2mL的水,以防过滤时硝酸钾晶体过早析出 |
| D、为了加快反应速率得到较干燥的硅酸白色胶状沉淀可以采用抽滤的方法 |
 酚酞,别名非诺夫他林,是制药工业原料:适用于习惯性顽固便秘,有片剂、栓剂等多种剂型,其结构如右图所示,有关酚酞说法不正确的是( )
酚酞,别名非诺夫他林,是制药工业原料:适用于习惯性顽固便秘,有片剂、栓剂等多种剂型,其结构如右图所示,有关酚酞说法不正确的是( )| A、分子式为C20H14O4 |
| B、可以发生取代反应、加成反应、氧化反应 |
| C、含有的官能团有羟基、酯基 |
| D、1mol该物质可与H2和溴水发生反应,消耗H2和Br2的最大值为10mol和4mol |
胡妥油(D)用作香料的原料,它可由A合成得到:

下列说法正确的是( )

下列说法正确的是( )
| A、若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于加成反应 |
| B、有机物D分子中所有碳原子一定共面 |
| C、有机物C 的所有同分异构体中不可有芳香族化合物存在 |
| D、有机物B 既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体 |
向20mL 0.5mol/L的氨水中逐滴加入等物质的量浓度的盐酸,测定混合溶液的温度变化如图所示.下列关于混合溶液的说法错误的是( )


| A、从a点到b点,混合溶液不可能存在:c(Cl-)=c(NH4+) |
| B、由水电离的c(H+):b点>c点 |
| C、氨水的电离平衡常数:b点>a点 |
| D、b焦到c点,混合溶液中可能存在:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |

