题目内容
17.按要求写出相应的方程式(1)FeSO4的电离方程式FeSO4=Fe2++SO42-.
(2)Na在空气中点燃的化学方程式2Na+O2$\frac{\underline{\;加热\;}}{\;}$Na2O2.
(3)Al(OH)3溶解于NaOH溶液的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
分析 (1)FeSO4能电离为Fe2+和SO42-;
(2)钠在空气中燃烧生成过氧化钠;
(3)Al(OH)3溶解于NaOH溶液后生成NaAlO2和水.
解答 解:(1)FeSO4能电离为Fe2+和SO42-,故FeSO4的电离方程式为:FeSO4=Fe2++SO42-,故答案为:FeSO4=Fe2++SO42-;
(2)钠在空气中燃烧生成过氧化钠:2Na+O2$\frac{\underline{\;加热\;}}{\;}$Na2O2,故答案为:2Na+O2$\frac{\underline{\;加热\;}}{\;}$Na2O2;
(3)Al(OH)3溶解于NaOH溶液后生成NaAlO2和水,离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查了电离方程式和化学方程式以及离子方程式的书写,难度不大,应注意的是钠燃烧生成过氧化钠.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
8.下列试剂保存正确的是( )
| A. | 氯水保存在棕色细口瓶中 | B. | NaOH保存在具有玻璃塞的细口瓶中 | ||
| C. | 金属钠保存在CCl4中 | D. | 氢氟酸保存在玻璃塞的细口瓶中 |
5.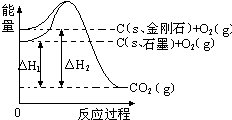 如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
 如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )
如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )| A. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 石墨和金刚石是同分异构体 |
12.下列各组离子,在水溶液中能大量共存的是( )
| A. | Na+、Ag+、Cl- | B. | Ba2+、H+、CO32- | C. | K+、Al3+、OH- | D. | Na+、Cl-、NO3- |
2.苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味.”按照现代科技观点,该文中的“气”是指( )
| A. | 脱落酸 | B. | 乙烯 | C. | 生长素 | D. | 甲烷 |
9.CoCl2•6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:
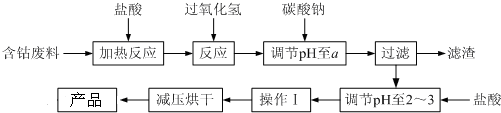
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少氮氧化合物等有毒气体的排放,防止产品中混有硝酸盐.
(2)加入过氧化氢的作用是将Fe2+氧化成Fe3+.
(3)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(4)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是样品中含有NaCl杂质(或烘干时失去了部分结晶水).

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少氮氧化合物等有毒气体的排放,防止产品中混有硝酸盐.
(2)加入过氧化氢的作用是将Fe2+氧化成Fe3+.
(3)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(4)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是样品中含有NaCl杂质(或烘干时失去了部分结晶水).
2.甲、乙、丙、丁四种化合物在常温下均成气态,且均由两种相同的短周期元素组成,它们的分子中所含电子数如下表,下列关于四种物质的推断正确的是( )
| 分子代号 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 16 | 18 | 26 |
| A. | 四种气体中至少有两种气体分子互为同分异构体 | |
| B. | 四种气体通入溴的四氯化碳溶液中,都能使其褪色 | |
| C. | 气体乙的分子内所有的原子在同一平面上 | |
| D. | 鉴别丙和丁两种气体,可以用高锰酸钾酸性溶液 |