题目内容
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+H+下列说法正确的是( )
| A、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| B、H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| C、在H2O2分解过程中,溶液的pH逐渐下降 |
| D、H2O2生产过程中加入少量Fe2+可以提高产率 |
考点:铁盐和亚铁盐的相互转变,过氧化氢
专题:元素及其化合物
分析:反应2Fe2++H2O2+2H+═2Fe3++2H2O中,Fe2+被H2O2氧化生成Fe3+,
反应2Fe3++H2O2═2Fe2++O2↑+2H+中,Fe3+被H2O2还原生成Fe2+,Fe2+可为H2O2分解的催化剂,以此解答.
反应2Fe3++H2O2═2Fe2++O2↑+2H+中,Fe3+被H2O2还原生成Fe2+,Fe2+可为H2O2分解的催化剂,以此解答.
解答:
解:A.总反应为2H2O2═2H2O+O2↑,Fe2+为H2O2分解的催化剂,Fe2+和Fe3+的总量保持不变,故A正确;
B.反应2Fe2++H2O2+2H+═2Fe3++2H2O中,Fe2+被H2O2氧化生成Fe3+,故H2O2的氧化性比Fe3+强;反应2Fe3++H2O2═2Fe2++O2↑+2H+中,Fe3+被H2O2还原生成Fe2+,故H2O2的还原性比Fe2+强,故B错误;
C.总反应为2H2O2═2H2O+O2↑,溶液的pH基本不变,故C错误;
D.Fe2+为H2O2分解的催化剂,可导致H2O2分解,所以H2O2生产过程要严格避免混入Fe2+,故D错误;
故选A.
B.反应2Fe2++H2O2+2H+═2Fe3++2H2O中,Fe2+被H2O2氧化生成Fe3+,故H2O2的氧化性比Fe3+强;反应2Fe3++H2O2═2Fe2++O2↑+2H+中,Fe3+被H2O2还原生成Fe2+,故H2O2的还原性比Fe2+强,故B错误;
C.总反应为2H2O2═2H2O+O2↑,溶液的pH基本不变,故C错误;
D.Fe2+为H2O2分解的催化剂,可导致H2O2分解,所以H2O2生产过程要严格避免混入Fe2+,故D错误;
故选A.
点评:本题考查氧化还原反应以及化学反应的探究,题目难度中等,注意从化合价的角度分析氧化还原反应.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列离子方程式不正确的是( )
| A、敞开体系,向FeCl2溶液滴加NaOH:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ |
| B、酸性 FeSO4 溶液中加 H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C、硫代硫酸钠溶液中加入稀硫酸:2H++S2O3-=S↓+SO2↑+H2O |
| D、将氧气通入酸性碘化钾溶液中:2I-+O2+4H+=I2+2H2O |
下列关于实验原理或操作的叙述中,不正确的是( )
| A、判断皂化反应是否完全,可取反应后的混合液滴入热水中 |
| B、减压过滤不宜过滤胶状沉淀或颗粒太小的沉淀 |
| C、制备硫酸亚铁铵晶体,需加热至大量晶体析出并剩余少量液体即停止加热 |
| D、易燃试剂与强氧化性试剂需分开放置,并远离火源;金属着火时可用细沙覆盖灭火 |
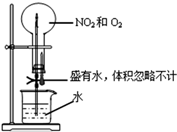 用如图装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑
用如图装置做喷泉实验,该实验条件下的气体摩尔体积为a L/mol,且不考虑2NO2?N2O4.最终液体充满了烧瓶,则烧瓶内溶液的物质的量浓度约是( )
A、
| ||
B、
| ||
C、
| ||
| D、无法计算 |