题目内容
(1)①写出Na2SO4的电离方程式 .
②氧化铝和氢氧化钠溶液反应的离子反应方程式
③OH-+H+═H2O改写为化学方程式
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用,①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是 .
②氧化铝和氢氧化钠溶液反应的离子反应方程式
③OH-+H+═H2O改写为化学方程式
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用,①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序是
考点:离子方程式的书写,物质的分离、提纯和除杂
专题:
分析:(1)①硫酸钠完全电离,电离出钠离子和硫酸根离子;
②反应生成偏铝酸钠和水;
③为强酸与强碱生成可溶性盐和水的离子反应;
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,碳酸钠除去钙离子、氯化钡除去钡离子,NaOH除去镁离子,最后加盐酸除去碳酸钠,注意碳酸钠一定在氯化钡之后.
②反应生成偏铝酸钠和水;
③为强酸与强碱生成可溶性盐和水的离子反应;
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,碳酸钠除去钙离子、氯化钡除去钡离子,NaOH除去镁离子,最后加盐酸除去碳酸钠,注意碳酸钠一定在氯化钡之后.
解答:
解:(1)①硫酸钠完全电离,电离出钠离子和硫酸根离子,则电离方程式为Na2SO4═2Na++SO42-,故答案为:Na2SO4═2Na++SO42-;
②反应生成偏铝酸钠和水,离子反应为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
③为强酸与强碱生成可溶性盐和水的离子反应,反应如H2SO4+2NaOH═2H2O+Na2SO4,故答案为:H2SO4+2NaOH═2H2O+Na2SO4;
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,碳酸钠除去钙离子、氯化钡除去钡离子,NaOH除去镁离子,最后加盐酸除去碳酸钠,注意碳酸钠一定在氯化钡之后,则试剂的加入顺序为②③①④或③②①④,故答案为:②③①④或③②①④.
②反应生成偏铝酸钠和水,离子反应为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
③为强酸与强碱生成可溶性盐和水的离子反应,反应如H2SO4+2NaOH═2H2O+Na2SO4,故答案为:H2SO4+2NaOH═2H2O+Na2SO4;
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,碳酸钠除去钙离子、氯化钡除去钡离子,NaOH除去镁离子,最后加盐酸除去碳酸钠,注意碳酸钠一定在氯化钡之后,则试剂的加入顺序为②③①④或③②①④,故答案为:②③①④或③②①④.
点评:本题考查离子反应方程式的书写及粗盐提纯,为高频考点,明确物质的性质、发生的反应及混合物分离提纯等即可解答,题目难度不大.

练习册系列答案
相关题目
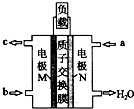 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )| A、燃料电池将化学能转化为电能 |
| B、a是甲醇,b是氧气 |
| C、质子从M电极区穿过交换膜移向N电极区 |
| D、负极反应:CH40-6e-+H20=C02↑+6H+ |
下列叙述中,正确的是( )
| A、溶度积大的化合物溶解度肯定大 |
| B、向含有AgCl固体的溶液中加入适量的水使溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变 |
| C、将难溶电解质放入水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积 |
| D、AgCl水溶液的导电性很弱,所以AgCl为弱电解质 |
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| B、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
下列物质的稀溶液中,溶质的阴、阳离子个数之比为2:1的是( )
| A、Na2HPO4 |
| B、NaHSO4 |
| C、(NH4)2SO4 |
| D、K2S |
下列说法中正确的是( )
| A、摩尔是用于计量微观粒子集体的物理量 |
| B、CO2的摩尔质量为44g |
| C、0.5mol水中约含6.02×1023个H |
| D、标准状况下1 mol任何物质体积均为22.4L |