题目内容
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
(2)鉴于H2O2弱酸性,它可以同强碱作用形成正盐,在一定条件下也可以形成酸式盐.请写出H2O2与Ba(OH)2作用形成正盐的化学方程式: .
(2)鉴于H2O2弱酸性,它可以同强碱作用形成正盐,在一定条件下也可以形成酸式盐.请写出H2O2与Ba(OH)2作用形成正盐的化学方程式:
考点:离子方程式的书写,物质的检验和鉴别的基本方法选择及应用
专题:离子反应专题,元素及其化合物
分析:(1)双氧水可以可作是二元弱酸,说明双氧水分子能发生两步电离;
(2)H2O2与Ba(OH)2作用形成正盐为BaO2,同时生成水.
(2)H2O2与Ba(OH)2作用形成正盐为BaO2,同时生成水.
解答:
解:(1)双氧水可以可作是二元弱酸,说明双氧水分子能发生两步电离,其电离方程式为H2O2?H++HO2-、HO2-?H++O22-,
故答案为:H2O2?H++HO2-、HO2-?H++O22-;
(2)双氧水和氢氧化钡生成盐和水,反应方程式为H2O2+Ba(OH)2=BaO2+2H2O,故答案为:H2O2+Ba(OH)2=BaO2+2H2O.
故答案为:H2O2?H++HO2-、HO2-?H++O22-;
(2)双氧水和氢氧化钡生成盐和水,反应方程式为H2O2+Ba(OH)2=BaO2+2H2O,故答案为:H2O2+Ba(OH)2=BaO2+2H2O.
点评:本题以双氧水为载体考查了弱电解质的电离,明确弱电解质电离特点及电离方程式书写特点即可解答,注意利用知识迁移的方法解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
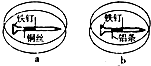 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是( )
| A、a中铁钉发生还原反应 |
| B、b中铁钉附近呈现红色 |
| C、a中铜丝附近呈现蓝色 |
| D、b中铝条附近有气泡产生 |
在25℃时,某稀溶液中由水电离产生的c(OH-)水=10-11mol/L.下列有关该溶液的叙述正确的是( )
| A、该溶液一定呈酸性 |
| B、该溶液中的c(H+)肯定等于10-3mol/L |
| C、该溶液的pH可能为3,可能为11 |
| D、该溶液一定呈碱性 |
在25℃时,100ml1.0mol/L的盐酸与等体积1.2mol/L的氢氧化钠溶液混合,所得溶液的pH为( )
| A、7 | B、12 | C、13 | D、无法计算 |
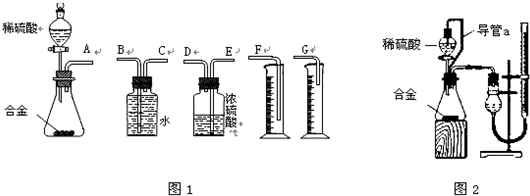
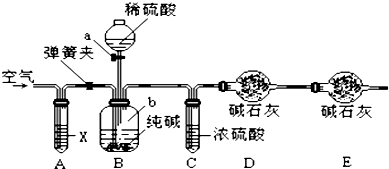
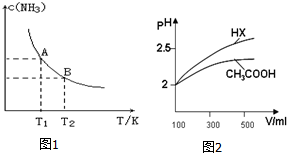 (1)根据最新“人工固氮”的研究报道,在常温常压和光照条件下N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)=4NH3(g)+3O2(g).若已知:
(1)根据最新“人工固氮”的研究报道,在常温常压和光照条件下N2在催化剂表面与水发生反应:2N2(g)+6H2O(l)=4NH3(g)+3O2(g).若已知: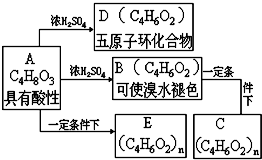 化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.
化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.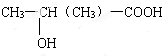 .
.