题目内容
下列各原子或离子的电子排布式错误的是( )
| A、Na+ 1s22s22p6 |
| B、O2- 1s22s22p6 |
| C、Si 1s22s22p2 |
| D、Al 1s22s22p63s23p1 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:原子核外电子排布应符合构造原理、能量最低原理、洪特规则和泡利不相容原理,一般来说离子的核外最外层达到8电子稳定结构,根据构造原理,s能级最多可容纳2个电子,p能级有3个轨道最多可容纳6个电子,电子总是优先从能量低的能层、能级排列,其中s2是原子得两个电子形成的稳定的结构,所以第三能层中的电子排布最多应为3s23p6,据此分析解答.
解答:
解:A.Na的原子序数为11,离子的核外电子排布式为1s22s22p6,最外层达到8电子稳定结构,故A正确;
B.O原子核外有8个电子,O2-核外电子排布式为1s22s22p6,最外层达到8电子稳定结构,故B正确;
C.Si原子核外有14个电子,核外电子排布式为:1s22s22p63s23p2,故C错误;
D.Al原子核外有13个电子,Al原子核外电子排布式为1s22s22p63s23p1,故D正确;
故选C.
B.O原子核外有8个电子,O2-核外电子排布式为1s22s22p6,最外层达到8电子稳定结构,故B正确;
C.Si原子核外有14个电子,核外电子排布式为:1s22s22p63s23p2,故C错误;
D.Al原子核外有13个电子,Al原子核外电子排布式为1s22s22p63s23p1,故D正确;
故选C.
点评:本题考查了原子或离子核外电子排布,明确排布规律及其规则是解本题关键,为考试热点,知道每个能级最多排列的电子数,要遵循构造原理,题目难度不大.

练习册系列答案
相关题目
将2mol SO2和0.5mol O2放置于密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g),充分反应后,生成的SO3的物质的量可能是( )
| A、0.8mol |
| B、1mol |
| C、1.5mol |
| D、2mol |
下列说法不正确的是( )
| A、在有盐桥构成的铜-锌-稀硫酸原电池中,盐桥中的阳离子移向电池的锌极 |
| B、化学平衡的建立与途径无关,可以从正反应方向建立,也可以从逆反应方向建立 |
| C、可以借助分光度计采用比色的方法测定某反应的化学反应速率 |
| D、在FeCl3与过量的KI溶液充分反应后的溶液用CCl4萃取后,往上层溶液中加入几滴KSCN溶液,溶液出现血红色,说明该化学反应存在限度 |
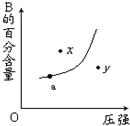 对于mA(s)+nB(g)?pC(g)△H<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
对于mA(s)+nB(g)?pC(g)△H<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、n<p |
| C、a点时增加A的物质的量,B的百分含量减小 |
| D、x点的状态是v正>v逆 |
下列四个选项是在不同的情况下对化学反应A(g)+3B(g)?2C(g)+2D(g)测得的用不同物质表示的反应速率,其中表示该化学反应的反应速率最快的是( )
| A、v(D)=0.6 mol?L-1?min-1 |
| B、v(A)=0.2 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(B)=0.45 mol?L-1?s-1 |
某浓度的铬酸溶液(H2CrO4),向其中加入少量碱以调节pH值(忽略溶液体积变化),下表为各离子浓度(mol/L)与pH之间的关系如下表,下列说法不正确的是( )
| pH | [H2CrO4] | [HCrO4-] | [CrO42-] | [Cr2O72-] |
| 4 | 0 | 0.095 | 0.035 | 0.435 |
| 7 | 0 | 0.086 | 0.274 | 0.320 |
| 10 | 0 | 0.004 | 0.990 | 0.003 |
| A、铬酸的电离方程式为H2CrO4═2H++CrO42- |
| B、铬酸的总浓度为1mol/L |
| C、[H+]越大,HCrO4-浓度越大 |
| D、已知Cr2O72-为橙色离子,CrO42-为黄色离子,随着pH的升高溶液将逐渐变为黄色 |