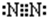题目内容
(2004·上海)下列叙述正确的是
[ ]
A.碳酸钙难溶于水,放入水中水溶液不导电,且碳酸钙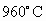 时分解不存在熔融状态导电的性质,故
时分解不存在熔融状态导电的性质,故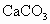 是非电解质
是非电解质
B.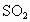 溶于水后得到水溶液导电,所以
溶于水后得到水溶液导电,所以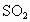 是电解质
是电解质
C.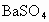 在水中溶解度很小,但被溶解部分全部电离了,所以
在水中溶解度很小,但被溶解部分全部电离了,所以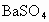 是强电解质
是强电解质
D.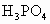 晶体在熔融状态下不导电,但溶于水后其水溶液导电,故
晶体在熔融状态下不导电,但溶于水后其水溶液导电,故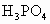 是电解质
是电解质
答案:CD
解析:
解析:
|
解析:电解质在熔化状态或水溶液中能导电,只是外表的现象是宏观判断的一种方法.其导电的根本在于化合物在这种条件下电离了,产生自由移动的离子,而且只有离子浓度达到一定程度才能表现出“导电”这一宏观现象.因此判断一化合物是否为电解质关键是看它是否能发生电离.而且离子是它本身电离出来的,不能是化合物与水反应生成新化合物电离出离子 (如 , ,   ,而 ,而 不能电离出离子),故A、B判断不对. 不能电离出离子),故A、B判断不对. 虽难溶,但溶解部分完全电离应是强电解质, 虽难溶,但溶解部分完全电离应是强电解质, 是非电解质. 是非电解质. |

练习册系列答案
相关题目
 (2004?上海)在一定条件下,二氧化硫和氧气发生如下反应:
(2004?上海)在一定条件下,二氧化硫和氧气发生如下反应: