题目内容
9.常温下,氨水与硫酸铵的混合液pH=7时,c(SO42-)与 c(NH4+)之比为( )| A. | 等于1:2 | B. | 小于1:2 | C. | 等于2:1 | D. | 大于2:1 |
分析 pH=7时c(OH-)=c(H+),存在电荷守恒式为c(OH-)+2 c(SO42-)=c(NH4+)+c(H+),以此来解答.
解答 解:pH=7时c(OH-)=c(H+),由c(OH-)+2 c(SO42-)=c(NH4+)+c(H+)可知,2 c(SO42-)=c(NH4+),则c(SO42-)与 c(NH4+)之比为1:2,
故选A.
点评 本题考查离子浓度的关系,为高频考点,把握pH=7及电荷守恒式为解答的关键,侧重分析与应用能力的考查,注意电荷守恒的应用,题目难度不大.

练习册系列答案
相关题目
19.设NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 1L0.1mol/L的NaHCO3溶液中,HCO3-、CO32-离子数之和为0.1NA | |
| B. | 44gCO2、N2O组成的混合气体中所含有的原子数为3NA | |
| C. | 36H2中含有的中子数目为24NA | |
| D. | 2.24L(标准状况)O2与钠反应时,转移电子数目可能为0.3NA |
20.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | CO2通入NaClO 溶液中能生成HClO |
| B | 根据溶液的pH与溶液碱性的关系 | pH=6.8的溶液一定显酸性 |
| C | 组成和结构相似的物质,沸点随相对分子质量增大而升高 | H2O沸点低于H2S |
| D | 同主族元素从上至下非金属性减弱 | HF、HCl、HBr、HI的酸性依次减弱 |
| A. | A | B. | B | C. | C | D. | D |
17.下列有关有机化合物结构和性质的说法正确的是( )
| A. | 乙烯、苯和乙酸均能发生加成反应 | |
| B. | 某芳香烃的分子式为C10H14,它可使酸性 KMnO4溶液褪色,且分子结构中只有一个侧链,符合条件的烃有4种 | |
| C. | 1 mol的有机物(结构如图)最多能与含5mol NaOH的水溶液完全反应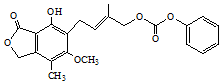 | |
| D. | 油脂皂化反应得到高级脂肪酸与甘油 |
4.氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液.下列说法正确的是( )
| A. | 负极反应为:2H2+4OH--4e-═4H2O | |
| B. | 正极反应为:O2+4H++4e-═2 H2O | |
| C. | 电池工作时溶液中的阴离子移向正极 | |
| D. | 电池工作时负极区pH升高,正极区pH下降 |
14.对于强碱性条件的甲醇燃料电池,下列说法正确的是( )
| A. | 负极反应式:CH3OH-8e-+8OH-=CO2+6H2O | |
| B. | 电池工作时,CH3OH发生还原反应,被氧化 | |
| C. | 电池工作时,溶液中的阴离子向负极移动 | |
| D. | 电池工作一段时间后,溶液的pH增大 |
18.各指定粒子数目不等于阿伏加德罗常数值的是( )
| A. | 1g H2 所含的原子个数 | |
| B. | 4g 氦气所含的原子个数 | |
| C. | 23g 金属 Na 全部转变为金属离子时失去的电子个数 | |
| D. | 16g O2 所含的分子个数 |