题目内容
16.常温下,下列溶液中有关微粒的物质的量浓度关系正确的是( )| A. | 0.1 mol•L-1 (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+) | |
| B. | 0.1 mol•L-1 NaHCO3溶液:c(OH-)=c(H+)+2c(H2CO3)+c(HCO3-) | |
| C. | 0.1 mol•L-1Na2S溶液:2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| D. | pH=12的NaOH溶液与等体积pH=2的醋酸混合后的溶液:c (CH3COO-)+c (OH-)=c (Na+)+c (H+) |
分析 A.铵根离子部分水解,导致铵根离子浓度减小,由于化学式(NH4)2Fe(SO4)2中含有1个亚铁离子,则亚铁离子的浓度最小;
B.根据碳酸氢钠溶液中的质子守恒判断;
C.根据硫化钠溶液中的物料守恒判断;
D.该溶液中满足电荷守恒,根据电荷守恒判断.
解答 解:A.0.1 mol•L-1 (NH4)2Fe(SO4)2溶液中,铵根离子部分水解,则c(SO42-)>c(NH4+),由于化学式(NH4)2Fe(SO4)2中含有1个Fe2+子,则c(NH4+)>c(Fe2+),溶液中离子浓度大小为:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+),故A正确;
B.0.1 mol•L-1 NaHCO3溶液中,根据质子守恒可得:c(CO32-)+c(OH-)=c(H+)+c(H2CO3),故B错误;
C.0.1 mol•L-1Na2S溶液中,根据物料守恒可得:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),故C错误;
D.pH=12的NaOH溶液与等体积pH=2的醋酸混合后的溶液,根据电荷守恒可得:c (CH3COO-)+c (OH-)=c (Na+)+c (H+),故D正确;
故选AD.
点评 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒及质子守恒的含义为解答关键,注意掌握盐的水解原理及其应用方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
6.元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是(填离子符号)Na+.
(3)已知:
①工业制镁时,电解MgCl2而不电解MgO的原因是MgO的熔点高,熔融时消耗更多能量,增加生产成本;
②制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电; ③写出电解Al2O3反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$+4Al+3O2↑.
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是(填离子符号)Na+.
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
②制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电; ③写出电解Al2O3反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$+4Al+3O2↑.
7.下列物质没有固定沸点的是( )
| A. | 氯仿 | B. | 汽油 | C. | 硝基苯 | D. | 甲醇 |
4.下列各组物质中,互称为同分异构体的是( )
| A. | 水与冰 | B. | O2与O3 | C. | 丁烷和正丁烷 | D. | 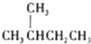 与 与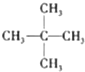 |
11.有关苯的结构和性质,下列说法正确的是( )
| A. | 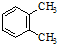 与 与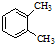 是同分异构体 是同分异构体 | |
| B. | 苯可以发生加成反应 | |
| C. | 可通过萃取的方法,从煤中提取苯 | |
| D. | 向2mL苯中加入1mL酸性高锰酸钾溶液,震荡后静置,可观察到液体分层,上层呈紫红色 |
1. 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
I.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释合理(填“合理”或“不合理)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
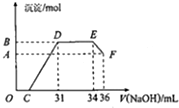
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示.
请回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O.
(2)B与A的差值为0.008mol,B点对应的沉淀的物质的量为0.032mol,C点对应的氢氧化钠溶液的体积为7ml.
 某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材(必修加选修)中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
II.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如图所示.
请回答下列问题:
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O.
(2)B与A的差值为0.008mol,B点对应的沉淀的物质的量为0.032mol,C点对应的氢氧化钠溶液的体积为7ml.
8.有关氯化铁溶液与氢氧化铁胶体说法正确的是( )
| A. | 分散质粒子直径在1~100nm之间 | B. | 可用丁达尔效应区别这两种物质 | ||
| C. | 能用过滤的方法将它们分离 | D. | 都呈红褐色 |
5.已知:
①CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
则CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)的△H为( )
①CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
则CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)的△H为( )
| A. | +478.7kJ•mol-1 | B. | -764.5 kJ•mol-1 | ||
| C. | -478.7kJ•mol-1 | D. | +764.5kJ•mol-1 |
6.下述实验设计能够达到目的是( )
| A. | SO2中混有少量SO3,通过足量浓硫酸,收集气体 | |
| B. | HNO3溶液中混有少量H2SO4,加入适量BaCl2溶液,再过滤 | |
| C. | 提取溴水中的溴,可用加入乙醇萃取的方法 | |
| D. | 检验溶液中是否含有Fe2+,向溶液中滴入氯水后,再滴加KSCN溶液 |