题目内容
11.已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A. | 乙的常见氧化物只有一种 | |
| B. | 气态氢化物稳定性:丙>丁 | |
| C. | 原子半径大小:戊<丙 | |
| D. | 丙的氧化物能与戊的氢化物的水溶液反应 |
分析 甲、丙的最低价都为-4价,应为第ⅣA族元素,且原子序数甲<丙,为短周期元素,则甲为C元素,丙为Si元素,短周期元素甲、乙、丙、丁、戊的原子序数依次增大,可知乙为Na元素,丁为S元素,戊为Cl元素,结合对应的单质、化合物的性质以及题目要求解答该题.
解答 解:甲、丙的最低价都为-4价,应为第ⅣA族元素,且原子序数甲<丙,为短周期元素,则甲为C元素,丙为Si元素,短周期元素甲、乙、丙、丁、戊的原子序数依次增大,可知乙为Na元素,丁为S元素,戊为Cl元素,
A.乙为Na,对应的氧化物有Na2O和Na2O2两种,故A错误;
B.非金属性Si<S,元素的非金属性越强,对应的氢化物越稳定,故B错误;
C.戊为Cl元素,丙为Si元素,同周期原子序数大的半径小,则原子半径大小:戊<丙,故C正确;
D.丙的氧化物为SiO2,戊的氢化物为HCl,二者不反应,故D错误;
故选C.
点评 本题考查原子结构与元素的性质,为高考常见题型,侧重于学生的分析能力的考查,注意从化合价的角度判断元素的种类,为解答该题的关键,把握元素的性质以及比较的角度,题目难度不大.

练习册系列答案
相关题目
1.下列化学用语表述正确的是( )
| A. | 甲烷分子的球棍模型: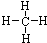 | B. | 氯化钠的电子式: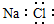 | ||
| C. | 氯气的比例模型: | D. | 硫离子的结构示意图: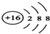 |
2.下列说法正确的是( )
| A. | SiO2溶于水显酸性 | |
| B. | CO2通入水玻璃中可得到硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2在常温下不与任何物质反应 |
19.下列有关合金的说法正确的是( )
| A. | 合金的硬度一般比它的成分金属大 | |
| B. | 合金的熔点一般比它的成分金属的熔点高 | |
| C. | 合金在工业上的用途比纯金属更广 | |
| D. | 生活中用量最大的合金是铁合金 |
6.下列关于能源和作为能源使用的物质的叙述中,错误的是( )
| A. | 化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 | |
| B. | 太阳能不能直接转化为电能 | |
| C. | 物质的化学能可以在不同条件下转化为热能、电能等为人类所用 | |
| D. | 绿色植物发生光合作用时,将太阳能转化为化学能“贮存”起来 |
16.1999年曾报导合成和分离了含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是( )
| A. | N5+共有34个核外电子 | |
| B. | N5+中氮氮原子间以共用电子对结合 | |
| C. | 化合物N5AsF6中As化合价为+1 | |
| D. | 化合物N5AsF6属于离子晶体 |
3.金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石.已知12g石墨完全转化为金刚石时,要吸收a kJ的能量,下列说法正确的是( )
①石墨不如金刚石稳定
②金刚石不如石墨稳定
③等质量的石墨和金刚石完全燃烧,金刚石放出的能量多
④石墨转化为金刚石是氧化还原反应.
①石墨不如金刚石稳定
②金刚石不如石墨稳定
③等质量的石墨和金刚石完全燃烧,金刚石放出的能量多
④石墨转化为金刚石是氧化还原反应.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
12.下列物质中含有非极性共价键的离子化合物是( )
| A. | Cl2 | B. | Na2O2 | C. | H2O2 | D. | MgCl2 |