题目内容
10.现有一份由炭粉、Fe2O3、CuO中的某几种物质组成的混合物粉末,某校化学课外小组取样品进行了如下实验:
(1)可以确定该样品中一定存在C,CuO(填化学式).
(2)若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式为C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(3)向Y溶液和固体混合物中通入过量的Cl2,并不断搅拌,充分反应后,则溶液中的阳离子是H+、Fe3+、Cu2+.
分析 (1)能与Fe2O3、CuO、C物质反应产生两种气体的浓酸不可能是浓盐酸;如果是浓硫酸,可以与C单质发生氧化还原反应,浓硫酸被还原为SO2,C被氧化为CO2,如果是浓硝酸,则两种气体是CO2和NO2,其变化与加浓硫酸的反应相同.无论是那种浓酸均可以使两种氧化物Fe2O3、CuO转化为对应的盐,盐溶液加入过量的铁粉,可以得到红色的固体,即为铜,据此圈定含有的物质;
(2)浓酸若为浓硫酸,其与样品中的C反应生成CO2和SO2,通入NaHCO3溶液后SO2被吸收,剩余CO2;
(3)X溶液中加过量Fe粉,得Y溶液和两种固体(其中一种固体为红色的Cu,另一种为过量的Fe粉),这个过程发生了置换反应:Cu2++Fe═Cu+Fe2+;再向Y溶液中通入过量Cl2,则会发生反应:Cl2+2Fe2+═2Cl-+2Fe3+、2Fe3++Cu═2Fe2++Cu2+、Cl2+H2O=HCl+HClO.
解答 解:(1)与Fe2O3、Fe、CuO、C、Al物质反应产生两种气体的浓酸不可能是浓盐酸;如果是浓硫酸,可以与Fe、C、Al单质发生氧化还原反应,浓硫酸被还原为SO2,C被氧化为CO2,Fe和Al被氧化为Fe3+和Al3+;如果是浓硝酸,则两种气体是CO2和NO2,其变化与加浓硫酸的反应相同.无论是那种浓酸均可以使两种氧化物Fe2O3、CuO转化为对应的盐,盐溶液加入过量的铁粉,可以得到红色的固体,即为铜,据此得到该样品中一定存在C,CuO,故答案为:C,CuO;
(2)浓酸若为浓硫酸,其与样品中的C反应生成CO2和SO2,通入NaHCO3溶液后SO2被吸收,剩余CO2,反应I中能同时生成两种气体的化学方程式是:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)向溶液X中加过量Fe粉,得Y溶液和两种固体,且一种固体为红色(Cu),另一种就是过量的Fe粉,这个过程发生了置换反应:Cu2++Fe=Cu+Fe2+,向Y溶液中通入过量氯气,并不断搅拌,会发生如下反应:Cl2+2Fe2+=2Cl-+2Fe3+,2Fe3++Cu=2Fe2++Cu2+,Cl2+H2O=HCl+HClO,充分反应后,溶液中的阳离子是:Cu2+、Fe3+、H+(特别注意没有了Fe2+),
故答案为:Cu2+、Fe3+、H+.
点评 本题考查无机推断,主要涉及金属单质、金属氧化物、非金属单质的性质,题目综合性强,涉及知识面广,难度中等,注意掌握浓硫酸、浓硝酸的性质.

| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 4:3 |
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 生成白色沉淀 |
| ② | A+C | 放出无色气体 |
| ③ | A+D | 放出无色气体 |
| ④ | B+C | 无明显变化 |
| ⑤ | B+D | 生成白色沉淀 |
| ⑥ | C+D | 无明显变化 |
根据实验现象,回答下列问题:
(1)A为Na2CO3溶液,C为稀盐酸.
(2)写出下列反应的离子方程式
A+BCO32-+Ba2+=BaCO3↓,A+DCO32-+2H+=CO2↑+H2O,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,反应后得到的溶液中含有的阴离子有OH-.
(4)上述没有明显变化的实验④、⑥,其中④发生了离子反应,离子方程式为H++OH-=H2O.请设计实验证明其发生了反应取少量Ba(OH)2溶液滴入几滴酚酞试液,溶液显红色,向该红色溶液中加入稀盐酸至过量,溶液变为无色,说明酸碱发生反应.(试剂任选)
 .
.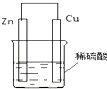 能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题: