题目内容
某温度时,某反应达到平衡,平衡常数K=
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A.该反应是焓变为正值,熵变为零 | ||||
| B.恒温恒容下,增大压强,H2浓度一定减小 | ||||
| C.升高温度,逆反应速率减小 | ||||
D.该反应化学方程式为CO+H2O
|
A.恒容时,温度升高,H2浓度减小,说明反应向正反应方向移动,则正反应为吸热反应,该反应是焓变为正值,由于反应前后气体的体积相等,则熵变为零,故A正确;
B.反应前后气体的体积相等,增大压强平衡不移动,恒温恒容下,增大压强,H2浓度一定增大,故B错误;
C.升高温度,正逆反应速率都增大,故C错误;
D.反应的化学方程式为CO2+H2
CO+H2O,故D错误,
故选A.
B.反应前后气体的体积相等,增大压强平衡不移动,恒温恒容下,增大压强,H2浓度一定增大,故B错误;
C.升高温度,正逆反应速率都增大,故C错误;
D.反应的化学方程式为CO2+H2
| ||
| △ |
故选A.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
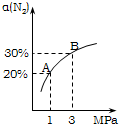 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )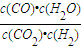 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )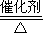 CO2+H2
CO2+H2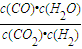 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )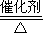 CO2+H2
CO2+H2