��Ŀ����
��������Ҫ�Ļ���ԭ�ϣ���ҵ������N2��H2�ϳ�NH3������ʽ���£�N2+3H2
2NH3
��1 ����֪NH3������CCl4��������װ���У������������հ�������
A�� B��
B��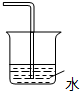 C��
C�� D��
D��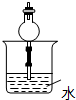
��2��ij�¶��£���һ����㶨Ϊ10L���ܱ�������ģ��ϳɰ���Ӧ������ʼʱ���룺0.1mol N2��0.1mol H2��0.2mol NH3�����ʱv�� v���������������=������֪���¶��£�ƽ�ⳣ��KֵΪ3.0��103����
��Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ������д�ʩ�п��е��� ������ĸ���ţ���
A��ѹ���������B���ʵ������¶�C��ͨ����������D������������
��3 ����˵��������Ӧ�ﵽƽ��״̬����
A��2�� ��H2��=3�ԣ�NH3��
B�����������ܶȲ��ٸı�
C����������ƽ����Է����������ٸı�
D����λʱ��������n mol N2��ͬʱ����2n mol NH3
��4 ����������ˮ������Һ�ڼ�ˮϡ�͵Ĺ����У���С�������С�����䡱����NH3?H2O�ĵ���̶� ������ƽ�ⳣ�� ����Һ��pHֵ ��
��5 ���������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5��ԭ������Һ�д���ƽ�� �������ӷ���ʽ��ʾ������ϡ��Һ��ˮ�ĵ����ԼΪ ��
| ���¸�ѹ |
| ���� |
��1 ����֪NH3������CCl4��������װ���У������������հ�������
A��
 B��
B�� C��
C�� D��
D��
��2��ij�¶��£���һ����㶨Ϊ10L���ܱ�������ģ��ϳɰ���Ӧ������ʼʱ���룺0.1mol N2��0.1mol H2��0.2mol NH3�����ʱv��
��Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ������д�ʩ�п��е���
A��ѹ���������B���ʵ������¶�C��ͨ����������D������������
��3 ����˵��������Ӧ�ﵽƽ��״̬����
A��2�� ��H2��=3�ԣ�NH3��
B�����������ܶȲ��ٸı�
C����������ƽ����Է����������ٸı�
D����λʱ��������n mol N2��ͬʱ����2n mol NH3
��4 ����������ˮ������Һ�ڼ�ˮϡ�͵Ĺ����У���С�������С�����䡱����NH3?H2O�ĵ���̶�
��5 ���������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5��ԭ������Һ�д���ƽ��
���㣺��ѧƽ���Ӱ������,���������ˮ��Һ�еĵ���ƽ��,ˮ�ĵ���
ר�⣺�����������������
��������1��������������ˮ��ֱ����ˮ���գ��ܹ��������������������հ���ʱ��ѡװ�ñ�����з�ֹ���������ã�A���õ��۵�©����C�����Ȼ�̼��D�и���ܶ�������ֹ����������
��2������Ũ�Ȼ���ƽ�ⳣ��K�Ĺ�ϵ�Ƚϣ���Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ�����ѹ�����ӷ�Ӧ��Ũ�Ⱦ��ɣ�
��3����Ӧ�ﵽƽ��״̬�����淴Ӧ������ȣ������Ũ�Ȳ��䣻
��4����ˮ��Һ��ˮϡ�ͺٽ����룬����̶������볣��ֻ���¶��йأ�ϡ������������Ũ�ȼ�С��
��5��NH4+ˮ����������Һ�����ԣ��������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5��������ʣ�࣬����ˮ�ĵ��룬�����ᷴӦ��ȫ���ٽ�ˮ�ĵ��룮
��2������Ũ�Ȼ���ƽ�ⳣ��K�Ĺ�ϵ�Ƚϣ���Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ�����ѹ�����ӷ�Ӧ��Ũ�Ⱦ��ɣ�
��3����Ӧ�ﵽƽ��״̬�����淴Ӧ������ȣ������Ũ�Ȳ��䣻
��4����ˮ��Һ��ˮϡ�ͺٽ����룬����̶������볣��ֻ���¶��йأ�ϡ������������Ũ�ȼ�С��
��5��NH4+ˮ����������Һ�����ԣ��������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5��������ʣ�࣬����ˮ�ĵ��룬�����ᷴӦ��ȫ���ٽ�ˮ�ĵ��룮
���
�⣺��1��A�����۵�©��ʹNH3�������ͬʱ��ֹ��������ķ�������A����
B������NH3������ˮ���ɷ������������ܹ���ˮֱ�����գ���B��ȷ��
C������NH3������CCl4��NH3��CCl4�Ӵ����������������ܹ��������հ�������C����
D�����ڸ���ܵ��ϲ����ܹ���ֹ��������ķ�������D����
�ʴ�Ϊ��B��
��2���ϳɰ���ӦŨ�Ȼ�=
=
=40000��ƽ�ⳣ��K=3.0��103������ƽ�������ƶ���v����v����
��Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ�����ѹ�����ӷ�Ӧ��Ũ�Ⱦ��ɣ�
A��ѹ�����������ѹǿ����Ӧ��������ƽ�������ƶ�����A��ȷ��
B���ʵ������¶ȣ�ƽ�������ƶ�����B����
C��ͨ��������������Ӧ��Ũ������Ӧ��������ƽ�������ƶ�����C��ȷ��
D��������������ƽ�ⲻ�ƶ�����D����
��ѡAC��
�ʴ�Ϊ������AC��
��3�����ڷ�ӦN2+3H2?2NH3
A���κ�״̬�£��� ��H2�����ԣ�NH3��=3��2����A����
B��������������䣬����������������䣬����������ܶȲ��䣬��B����
C����ӦΪ���������С�ķ�Ӧ������������������䣬����������ƽ����Է����������ٸı䣬˵����Ӧ�ﵽƽ��״̬����C��ȷ��
D����λʱ��������n mol N2��ͬʱ����2n mol NH3��˵�����淴Ӧ������ȣ���D��ȷ��
�ʴ�Ϊ��CD��
��4����ˮ��Һ��ˮϡ�ͺٽ����룬����̶������볣��ֻ���¶��йأ��¶Ȳ��䣬���볣�����䣬ϡ�ͺ�����������Ũ�ȼ�С��PHֵ��С���ʴ�Ϊ�������䣻��С��
��5��NH4+ˮ����������Һ�����ԣ�ˮ�ⷽ��ʽΪNH4++H2O?NH3?H2O+H+���������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5����Һ��c��H+��=10-5��������ʣ�࣬����ˮ�ĵ��룬ˮ�������c��H+��=
=10-9�������ᷴӦ��ȫ���ٽ�ˮ�ĵ��룬ˮ�������c��H+��=10-5��
�ʴ�Ϊ��NH4++H2O?NH3?H2O+H+��10-9��10-5��
B������NH3������ˮ���ɷ������������ܹ���ˮֱ�����գ���B��ȷ��
C������NH3������CCl4��NH3��CCl4�Ӵ����������������ܹ��������հ�������C����
D�����ڸ���ܵ��ϲ����ܹ���ֹ��������ķ�������D����
�ʴ�Ϊ��B��
��2���ϳɰ���ӦŨ�Ȼ�=
| c2(NH3) |
| c(N2)?c3(H2) |
| 0.022 |
| 0.01��0.013 |
��Ҫ����Ӧ���ʣ���ƽ��������Ӧ�����ƶ�����ѹ�����ӷ�Ӧ��Ũ�Ⱦ��ɣ�
A��ѹ�����������ѹǿ����Ӧ��������ƽ�������ƶ�����A��ȷ��
B���ʵ������¶ȣ�ƽ�������ƶ�����B����
C��ͨ��������������Ӧ��Ũ������Ӧ��������ƽ�������ƶ�����C��ȷ��
D��������������ƽ�ⲻ�ƶ�����D����
��ѡAC��
�ʴ�Ϊ������AC��
��3�����ڷ�ӦN2+3H2?2NH3
A���κ�״̬�£��� ��H2�����ԣ�NH3��=3��2����A����
B��������������䣬����������������䣬����������ܶȲ��䣬��B����
C����ӦΪ���������С�ķ�Ӧ������������������䣬����������ƽ����Է����������ٸı䣬˵����Ӧ�ﵽƽ��״̬����C��ȷ��
D����λʱ��������n mol N2��ͬʱ����2n mol NH3��˵�����淴Ӧ������ȣ���D��ȷ��
�ʴ�Ϊ��CD��
��4����ˮ��Һ��ˮϡ�ͺٽ����룬����̶������볣��ֻ���¶��йأ��¶Ȳ��䣬���볣�����䣬ϡ�ͺ�����������Ũ�ȼ�С��PHֵ��С���ʴ�Ϊ�������䣻��С��
��5��NH4+ˮ����������Һ�����ԣ�ˮ�ⷽ��ʽΪNH4++H2O?NH3?H2O+H+���������ᷴӦ�õ���Σ�ij��NH4��2SO4ˮ��Һ��pH=5����Һ��c��H+��=10-5��������ʣ�࣬����ˮ�ĵ��룬ˮ�������c��H+��=
| 10-14 |
| 10-5 |
�ʴ�Ϊ��NH4++H2O?NH3?H2O+H+��10-9��10-5��
���������⿼���Ϊ�ۺϣ��漰��ѧƽ��״̬���жϡ�����ˮ�⡢ˮ�ĵ����֪ʶ��Ϊ�߿��������ͣ��Ѷ��еȣ�ע�������ػ������۵������Ӧ�ã�

��ϰ��ϵ�д�
 ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
�����Ŀ
�û����������ȡH2SO4������H2SO4������ȡ���ʣ�NH4��2SO4�����պ�FeS280.2%�Ļ�����75.0t������������79.2t��NH4��2SO4����֪NH3��������Ϊ92.6%��H2SO4��������Ϊ89.8%�������������ȡH2SO4ʱ����ʧ��Ϊ��������
| A��23.8% |
| B��33.4% |
| C��35.6% |
| D��63.8% |
һ����Na2O2��һ������CO2��Ӧ��Ĺ�������18.4g��ǡ����400mL 1mol?L-1��ϡ������ȫ��Ӧ������˵���������ǣ�NA��ʾ����٤����������������
| A����Ӧ�е���ת����Ϊ0.2NA |
| B��һ������CO2Ϊ0.1NA |
| C��18.4 g��������Ϊ0.1mol Na2CO3��0.1molNa2O2�Ļ���� |
| D��һ������Na2O2Ϊ0.1mol |
 ��
�� ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣�
ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣� e��
e�� f��
f��
