题目内容
13.关于C+CO2═2CO的反应,下列说法正确的是( )| A. | 单质C中C的化合价升高,被还原,是氧化剂 | |
| B. | CO2中C的化化合价降低,被氧化,CO2是还原剂 | |
| C. | CO既是氧化产物又是还原产物 | |
| D. | 是化合反应,不是氧化还原反应 |
分析 反应C+CO2=2CO中只有C元素化合价发生变化,C元素化合价分别由0价、+4价变化为+2价,以此解答该题.
解答 解:反应C+CO2=2CO中只有C元素化合价发生变化,C元素化合价分别由0价、+4价变化为+2价,质C中C的化合价升高,被氧化,CO2中C的化合价降低,被还原,CO既是氧化产物又是还原产物.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重考查基本概念,明确元素化合价与氧化剂和还原剂关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
4.下列的叙述中,不正确的是( )
| A. | SO2的摩尔质量是64 g/mol | |
| B. | 常温常压下,64 g SO2中所含的原子数为3×6.02×1023 个 | |
| C. | 1 mol SO3的质量是80 g | |
| D. | 标准状况下,1 mol SO3的体积为22.4 L |
1.在298K、1.01×105Pa下,将22g CO2缓慢通入750mL 1mol•L-1NaOH溶液中充分反应后,测得反应放热为x kJ.已知该条件下,1mol CO2缓慢通入1L 2mol•L-1NaOH溶液中充分反应后放热为y kJ.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x)kJ•mol-1 | |
| B. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| C. | CO2 (g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| D. | 2CO2 (g)+2NaOH(aq)═2NaHCO3(aq)△H=-(8x-y) kJ•mol-1 |
8.某硫原子的质量是ag,12C原子的质量是bg,若NA只表示阿伏加德罗常数的数值,则下列说法中正确的是( )
①该硫原子的相对原子质量为aNA
②mg该硫原子的物质的量为m/amol
③该硫原子的摩尔质量是aNAg•ml-1
④ag该硫原子所含有的电子数为16个.
①该硫原子的相对原子质量为aNA
②mg该硫原子的物质的量为m/amol
③该硫原子的摩尔质量是aNAg•ml-1
④ag该硫原子所含有的电子数为16个.
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ③④ |
5.已知18g CO和CO2的混合气体在标准状况下的体积为11.2L,则CO和CO2的分子数之比为( )
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 1:1 |
2.如图装置中,溶液体积均为200ml,开始时,电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过了0.02mol电子,若不考虑溶液体积的变化,下列叙述中正确的是( )
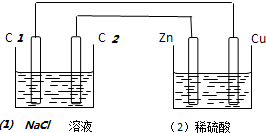

| A. | (1)中C2电极反应式为:2Cl--2e-═Cl2 | B. | (2)溶液中的SO42-向Cu极定向移动 | ||
| C. | (1)中滴入酚酞试液,C1极附近先变红 | D. | (2)中溶液的PH=1 |