题目内容
 实验室常用浓硝酸和浓硫酸的混合液与苯反应制取硝基苯.阅读下列材料回答有关问题.
实验室常用浓硝酸和浓硫酸的混合液与苯反应制取硝基苯.阅读下列材料回答有关问题.(1)写出实验室制取少量硝酸的化学方程式
(2)实验室用75%的硝酸来配制50mL65%的硝酸溶液,需用到的玻璃仪器有
实验室制硝基苯的过程如下:
(3)取一支大试管,将1.5mL浓硝酸和2mL浓硫酸混合配制混合酸,混合时应将浓硫酸滴加到浓硝酸中,且边滴边振荡,其目的是:
(4)在混合酸中慢慢滴加1mL苯,并不断摇匀.然后在60℃时加热10min.请在图中补完整该实验的装置图.
(5)反应结束后将混合液倒入另一只盛有水的烧杯中,在烧杯的底部可得到淡黄色的、有苦杏仁气味的油状液体;分离出此黄色油状液体的操作名称是
考点:制备实验方案的设计
专题:实验题
分析:(1)硝酸钠和浓硫酸微热反应生成硝酸和硫酸氢钠;
(2)根据溶液配制知识进分析,配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒,胶头滴管,具体步骤可概括为:计算、称量、溶解;
(3)浓硫酸溶于水温度升高,容易使液体飞溅,从热量散发防止硝酸分解分析;
(4)60℃时加热10min,需要水浴加热;
(5)生成的硝基苯和水溶液分层,分离方法用分液的方法分离;在烧杯的底部可得到淡黄色的、有苦杏仁气味的油状液体,使溶解了硝酸分解生成的二氧化氮气体,需要用氢氧化钠溶液洗涤得到无色的油状液体;
(2)根据溶液配制知识进分析,配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒,胶头滴管,具体步骤可概括为:计算、称量、溶解;
(3)浓硫酸溶于水温度升高,容易使液体飞溅,从热量散发防止硝酸分解分析;
(4)60℃时加热10min,需要水浴加热;
(5)生成的硝基苯和水溶液分层,分离方法用分液的方法分离;在烧杯的底部可得到淡黄色的、有苦杏仁气味的油状液体,使溶解了硝酸分解生成的二氧化氮气体,需要用氢氧化钠溶液洗涤得到无色的油状液体;
解答:
解:(1)实验室制取少量硝酸是利用硝酸钠和浓硫酸微热反应生成硝酸和硫酸氢钠,反应的化学方程式为:NaNO3+H2SO4(浓)
HNO3↑+NaHSO4;
故答案为:NaNO3+H2SO4(浓)
HNO3↑+NaHSO4;
(2)根据溶液配制知识进分析,计算需要的75%的硝酸溶液质量换算成溶液的体积,用量筒量取用胶头滴管定容后,在烧杯中加水溶解,配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒,胶头滴管,具体步骤可概括为:计算、称量、溶解;
故答案为:烧杯、量筒、玻璃棒、胶头滴管;
(3)浓硫酸溶于水温度升高,容易使液体飞溅,混合时应将浓硫酸滴加到浓硝酸中,且边滴边振荡,其目的是加快热量散发防止硝酸分解;
故答案为:防止硫酸溶于水时放出大量热,使液体飞溅;混合均匀,尽快散热,防止硝酸分解;
(4)60℃时加热10min,需要水浴加热,装置图为: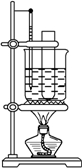 ;
;
故答案为: ;
;
(5)生成的硝基苯和水溶液分层,分离方法用分液的方法分离;在烧杯的底部可得到淡黄色的、有苦杏仁气味的油状液体,使溶解了硝酸分解生成的二氧化氮气体,需要用氢氧化钠溶液洗涤得到无色的油状液体;
故答案为:分液,氢氧化钠溶液;
| ||
故答案为:NaNO3+H2SO4(浓)
| ||
(2)根据溶液配制知识进分析,计算需要的75%的硝酸溶液质量换算成溶液的体积,用量筒量取用胶头滴管定容后,在烧杯中加水溶解,配制时使用的玻璃仪器主要是烧杯、量筒、玻璃棒,胶头滴管,具体步骤可概括为:计算、称量、溶解;
故答案为:烧杯、量筒、玻璃棒、胶头滴管;
(3)浓硫酸溶于水温度升高,容易使液体飞溅,混合时应将浓硫酸滴加到浓硝酸中,且边滴边振荡,其目的是加快热量散发防止硝酸分解;
故答案为:防止硫酸溶于水时放出大量热,使液体飞溅;混合均匀,尽快散热,防止硝酸分解;
(4)60℃时加热10min,需要水浴加热,装置图为:
 ;
;故答案为:
 ;
;(5)生成的硝基苯和水溶液分层,分离方法用分液的方法分离;在烧杯的底部可得到淡黄色的、有苦杏仁气味的油状液体,使溶解了硝酸分解生成的二氧化氮气体,需要用氢氧化钠溶液洗涤得到无色的油状液体;
故答案为:分液,氢氧化钠溶液;
点评:本题考查了实验制备物质的方法和原理分析,试剂选择和反应条件的准确掌握是解题关键,题目难度中等.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
下列事故或药品的处理正确的是( )
| A、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B、眼睛里溅进了少量酸或碱溶液,要立即用大量水冲洗,边洗边眨眼睛 |
| C、不慎洒出的酒精在桌上燃烧起来,应立即用大量水扑灭 |
| D、将含硫酸的废液倒入水槽,用水冲入下水道 |
 一定条件下,甲醇与水蒸气反应的化学方程式为:
一定条件下,甲醇与水蒸气反应的化学方程式为: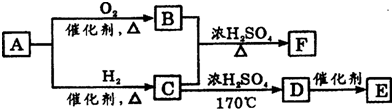
 在一烧杯中盛有20g CaCl2和NaCl的混合固体粉末,向其中逐滴滴加溶质的质量分数为10.6%的Na2CO3溶液,生成沉淀的质量与所滴入Na2CO3溶液的质量关系曲线如图所示.请根据题意回答下列问题:
在一烧杯中盛有20g CaCl2和NaCl的混合固体粉末,向其中逐滴滴加溶质的质量分数为10.6%的Na2CO3溶液,生成沉淀的质量与所滴入Na2CO3溶液的质量关系曲线如图所示.请根据题意回答下列问题: