题目内容
(1)在25°C时,纯水中C(H+)?C(OH-)= ;
(2)在NH4Cl溶液中C(H+) 10-7mol/L(大于、小于或等于),pH 7(大于、小于或等于);
(3)在Na2CO3溶液中C(H+) 10-7mol/L (大于、小于或等于),pH 7(大于、小于或等于)
(4)在NaCl溶液中C(H+) 10-7mol/L (大于、小于或等于),pH 7(大于、小于或等于).
(2)在NH4Cl溶液中C(H+)
(3)在Na2CO3溶液中C(H+)
(4)在NaCl溶液中C(H+)
考点:离子积常数,盐类水解的应用
专题:
分析:水的电离过程为H2O?H++OH-,在室温下其平衡常数为KW(25℃)=1.0×10-14,水电离出的氢离子浓度和氢氧根根离子浓度是相等的,酸、碱抑制水的电离,能水解的盐促进水的电离,据此回答.
解答:
解:(1)水的电离过程为H2O?H++OH-,在室温下其平衡常数为KW(25℃)=1.0×10-14,故答案为:1.0×10-14;
(2)在NH4Cl溶液中,铵根离子水解促进水的电离,水解显示酸性,c(H+)大于10-7mol/L,pH小于7,故答案为:大于;小于;
(3)在Na2CO3溶液中,碳酸根离子水解促进水的电离,水解显示碱性,c(H+)小于10-7mol/L,pH大于7,故答案为:小于;大于;
(4)在NaCl溶液中,水的电离平衡不受影响,所以c(H+)=10-7mol/L,pH=7,显示中性,故答案为:等于;等于.
(2)在NH4Cl溶液中,铵根离子水解促进水的电离,水解显示酸性,c(H+)大于10-7mol/L,pH小于7,故答案为:大于;小于;
(3)在Na2CO3溶液中,碳酸根离子水解促进水的电离,水解显示碱性,c(H+)小于10-7mol/L,pH大于7,故答案为:小于;大于;
(4)在NaCl溶液中,水的电离平衡不受影响,所以c(H+)=10-7mol/L,pH=7,显示中性,故答案为:等于;等于.
点评:本题考查学生水的电离以及水的电离平衡的影响因素等知识,注意水的离子积只受温度影响这一知识点,难度不大.

练习册系列答案
相关题目
下列叙述中,正确的是( )
| A、溶度积大的化合物溶解度肯定大 |
| B、向含有AgCl固体的溶液中加入适量的水使溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变 |
| C、将难溶电解质放入水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积 |
| D、AgCl水溶液的导电性很弱,所以AgCl为弱电解质 |
下列物质的稀溶液中,溶质的阴、阳离子个数之比为2:1的是( )
| A、Na2HPO4 |
| B、NaHSO4 |
| C、(NH4)2SO4 |
| D、K2S |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2.7g金属铝变成铝离子时,失去的电子数为0.1NA |
| B、常温常压下,NA个氮分子的质量为28g |
| C、8g甲烷中所含氢原子数为2NA |
| D、100mL2mol/L氯化铝溶液中含Cl-离子数为0.2NA |
下列烷烃的沸点是:甲烷:-162℃;乙烷:-89℃;丁烷:-1℃;戊烷:36℃.根据以上数字推断丙烷的沸点可能是( )
| A、约-40℃ |
| B、约-182℃ |
| C、约-108℃ |
| D、约56℃ |
下列说法中正确的是( )
| A、摩尔是用于计量微观粒子集体的物理量 |
| B、CO2的摩尔质量为44g |
| C、0.5mol水中约含6.02×1023个H |
| D、标准状况下1 mol任何物质体积均为22.4L |
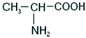 属于α-氨基酸);
属于α-氨基酸);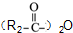 →
→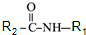 +R2COOH
+R2COOH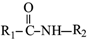 +NaOH→R1COONa+R2NH2
+NaOH→R1COONa+R2NH2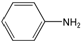 呈弱碱性,易被氧化
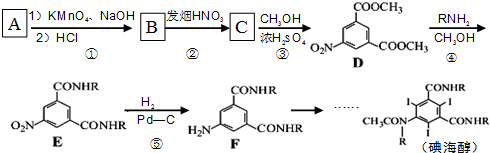
呈弱碱性,易被氧化 和(CH3CO)2O为原料制备染料中间体
和(CH3CO)2O为原料制备染料中间体 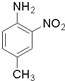 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).