题目内容
 科学研究表明,月球上可能存在少量水:月岩中含有钛铁矿,其主要成分的晶胞如图所示.
科学研究表明,月球上可能存在少量水:月岩中含有钛铁矿,其主要成分的晶胞如图所示.(1)钛铁矿中主要成分的化学式为
(2)基态铁原子的价电子排布式
(3)冰的密度比干冰(固态CO2)的密度小,其主要原因是
(4)水溶液中,H+主要以H3O+形式存在,H3O+中O原子的杂化轨道类型为
(5)Ti4+经多步反应得配合物[Ti(H2O)6]Cl3,1mol该配合物中含σ键的数目为
考点:晶胞的计算,原子核外电子排布,配合物的成键情况,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)根据均摊法,结合晶胞结构,可以确定化学式;
(2)铁是26号元素,核外电子排布为1s22s22p63s23p63d64s2;
(3)冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大,据此答题;
(4)H3O+中O原子的价电子对数为
=4,有三个H-O键,一对孤对电子,所以杂化轨道类型为sp3,离子的空间构型为三角锥形,根据等电子体原理,价电子数和原子数均相等的粒子互为等电子体,据此答题;
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为6+2×6=18,据此答题.
(2)铁是26号元素,核外电子排布为1s22s22p63s23p63d64s2;
(3)冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大,据此答题;
(4)H3O+中O原子的价电子对数为
| 6+3-1 |
| 2 |
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为6+2×6=18,据此答题.
解答:
解:(1)根据均摊法,结合晶胞结构,可知晶胞中含有氧原子数为12×
=3,钛原子数为8×
=1,铁原子数为1,所以化学式为FeTiO3,故答案为:FeTiO3;
(2)铁是26号元素,核外电子排布为1s22s22p63s23p63d64s2,故答案为:1s22s22p63s23p63d64s2;
(3)冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大,所以密度比干冰小,故答案为:冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大;
(4)H3O+中O原子的价电子对数为
=4,有三个H-O键,一对孤对电子,所以杂化轨道类型为sp3,离子的空间构型为三角锥形,根据等电子体原理,价电子数和原子数均相等的粒子互为等电子体,可写出等电子体为CH3-,故答案为:sp3;三角锥形;CH3-;
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为6+2×6=18,所以1mol配合物中含σ键的数目为18mol,故答案为:18mol.
| 1 |
| 4 |
| 1 |
| 8 |
(2)铁是26号元素,核外电子排布为1s22s22p63s23p63d64s2,故答案为:1s22s22p63s23p63d64s2;
(3)冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大,所以密度比干冰小,故答案为:冰中水分子之间有氢键,氢键具有方向性,所以分子之间的空隙较大;
(4)H3O+中O原子的价电子对数为
| 6+3-1 |
| 2 |
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为6+2×6=18,所以1mol配合物中含σ键的数目为18mol,故答案为:18mol.
点评:本题主要考查了均摊法计算晶胞的组成、核外电子排布、离子空间构型、配合物的结构等知识,综合性较强,难度中等.

练习册系列答案
相关题目
结合图判断,下列叙述正确的是( )


| A、Ⅰ和Ⅱ中正极均被保护 |
| B、Ⅰ和Ⅱ中负极反应均是:Fe-2e-═Fe2+ |
| C、Ⅰ正极反应是:O2+2H2O+4e-═4OH- |
| D、Ⅰ和Ⅱ中分别加入少量KSCN溶液,溶液均变红 |
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是次外层电子数的3倍,下列说法正确的是( )| A、原子半径:X<Z<W |
| B、非金属性:Y>Z |
| C、最高化合价:X<Y |
| D、最高价氧化物对应水化物的酸性:W>Z |
在100℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中.发生反应;2NO2(g)?N2O4(g)△H<0.反应过程中浓度变化如下:下列说法正确的是( )
| 容器 | 物质 | 起始浓度/(mol?L-1 | 平衡浓度/(mol?L-1 |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A、平衡后,分别压缩容器Ⅰ、Ⅱ,则Ⅰ、Ⅱ中气体颜色都将变深 |
| B、平衡时,Ⅰ、Ⅱ中反应物的转化率a(N2O4)<a(NO2) |
| C、平衡时,Ⅰ、Ⅱ中反应的平衡常数K(Ⅰ)═2K(Ⅱ) |
| D、平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ) |
 元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.
元素周期表揭示了化学元素间的内在联系,使其构成了一个完整的体系.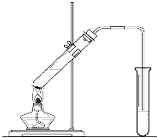 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: