题目内容
5.辣椒素酯类化合物的结构可以表示为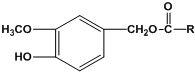 (R为烃基)
(R为烃基)其中一种辣椒素酯类化合物J的合成路线如下:
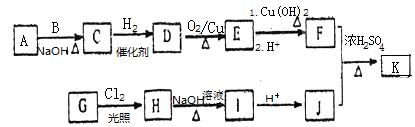
已知:
①A、B和E为同系物,其中B的摩尔质量为44g/mol,A和B核磁共振氢谱显示都有两组峰;
②化合物F的分子式为C7H14O2;
③
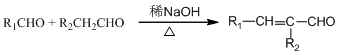
④化合物G分子式为C8H10O2;能使FeCl3溶液显紫色
回答下列问题:
(1)由D生产E的反应类型为氧化反应,E的化学名称为4,4-二甲基-1-戊醛.
(2)G中所含官能团的结构简式为羟基、醚键.
(3)写出由E生成F过程中①的离子方程式(CH3)3CCH2CH2CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$(CH3)3CCH2CH2COONa+Cu2O↓+3H2O;
(4)写出由H生成I的化学方程式为
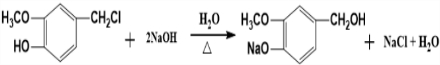 ,
,(5)若一次取样C,通过实验检验C中所含官能团,请按照实验的先后顺序写出试剂(用化学式表示)Ag(NH3)2OH溶液、稀HCl、Br2.
(6)G的所有同分异构体中,苯环上的一氯代物只有一种的共有8种(不考虑立体异构),写出核磁共振氢谱显示4组峰的任意一种结构的结构简式
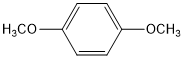 ,
,(7)根据以上信息,用B为原料,选择合适的有机试剂a,无机试剂和必要的条件合成甘油,写出试剂a的结构简式,按顺序析出①~④各步反应所加试剂盒反应条件.
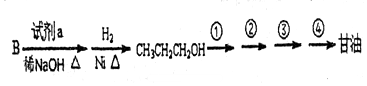
试剂a:HCHO①浓硫酸加热②高温、Br2③Br2④氢氧化钠的水溶液、加热.
分析 D氧化得到E、E氧化得到F,则D中存在-CH2OH结构,E含有-CHO,F含有-COOH,化合物F的分子式为C7H14O2,可知F为C6H13COOH.A、B和E为同系物,其中B的相对分子质量为44,则B为CH3CHO,A分子中碳原子数目为5,A的核磁共振氢谱显示有两组峰,则A为(CH3)3CCHO,A与B反应得到C,C与氢气反应得到D,则C为(CH3)3CCH=CHCHO,D为(CH3)3CCH2CH2CH2OH,E为(CH3)3CCH2CH2CHO,F为(CH3)3CCH2CH2COOH.G与氯气光照发生侧链烃基上取代反应生成H,H发生卤代烃水解反应得到I,又化合物G分子式为C8H10O2,能使FeCl3溶液显紫色,结合K的结构,则G为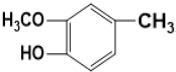 ,H为
,H为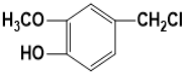 ,I为
,I为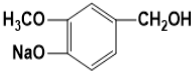 ,据此分析解答.
,据此分析解答.
(7)B为CH3CHO,根据信息③反应,CH3CHO与HCHO反应生成CH2=CHCHO,然后在与氢气加成生成CH3CH2CH2OH,CH3CH2CH2OH经过反应①发生消去反应生成CH3CH=CH2,CH3CH=CH2经过反应②在高温取代反应生成CH2BrCH=CH2,CH2BrCH=CH2经过反应③发生加成反应生成CH2BrCHBrCH2Br,CH2BrCHBrCH2Br经过反应④发生水解反应生成甘油,据此分析.
解答 解:(1)根据以上分析,由D生产E的反应类型为氧化反应,E为(CH3)3CCH2CH2CHO,化学名称为4,4-二甲基-1-戊醛,故答案为:氧化反应;4,4-二甲基-1-戊醛;
(2)G为 ,所含官能团的名称为羟基、醚键,故答案为:羟基、醚键;
,所含官能团的名称为羟基、醚键,故答案为:羟基、醚键;
(3)E为(CH3)3CCH2CH2CHO,则由E生成F过程中①的离子方程式(CH3)3CCH2CH2CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$(CH3)3CCH2CH2COONa+Cu2O↓+3H2O,故答案为:(CH3)3CCH2CH2CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$(CH3)3CCH2CH2COONa+Cu2O↓+3H2O;
(4)由H生成I的化学方程式为: ,
,
故答案为: ;
;
(5)C中含有醛基和碳碳双键,都能和溴水反应,要检验两种官能团,则应先用银氨溶液检验醛基,然后再用溴水检验碳碳双键,所以所加试剂先后顺序是:银氨溶液、稀盐酸、溴水,
故答案为:Ag(NH3)2OH溶液、稀HCl、Br2;
(6)G( )的同分异构体中,苯环上的一氯代物只有一种,可以含有2个-CH2OH且处于对位,或含有2个-OCH3且处于对位,可以含有4个取代基,为2个-OH、2个-CH3,当2个甲基相邻时,另外2个-OH分别与甲基相邻,或分别与甲基处于间位,当2个甲基处于间位时,另外2个-OH处于对位且分别与甲基相邻、相间,当2个甲基对位时,2个-OH分别与2个甲基相邻且2个羟基处于对位,或者2个羟基处于对位,或者2个-OH均与1个甲基相邻,故符合条件的同分异构共有8种,核磁共振氢谱显示2组峰的是
)的同分异构体中,苯环上的一氯代物只有一种,可以含有2个-CH2OH且处于对位,或含有2个-OCH3且处于对位,可以含有4个取代基,为2个-OH、2个-CH3,当2个甲基相邻时,另外2个-OH分别与甲基相邻,或分别与甲基处于间位,当2个甲基处于间位时,另外2个-OH处于对位且分别与甲基相邻、相间,当2个甲基对位时,2个-OH分别与2个甲基相邻且2个羟基处于对位,或者2个羟基处于对位,或者2个-OH均与1个甲基相邻,故符合条件的同分异构共有8种,核磁共振氢谱显示2组峰的是 ,
,
故答案为:8; ;
;
(7)B为CH3CHO,根据信息③反应,CH3CHO与HCHO反应生成CH2=CHCHO,所以试剂a为HCHO;然后在与氢气加成生成CH3CH2CH2OH,CH3CH2CH2OH经过反应①在浓硫酸加热条件下发生消去反应生成CH3CH=CH2,CH3CH=CH2经过反应②在高温条件下与Br2取代反应生成CH2BrCH=CH2,CH2BrCH=CH2经过反应③与Br2发生加成反应生成CH2BrCHBrCH2Br,CH2BrCHBrCH2Br经过反应④在氢氧化钠的水溶液中加热发生水解反应生成甘油,故答案为:HCHO;浓硫酸加热;高温、Br2;Br2;氢氧化钠的水溶液、加热.
点评 本题考查有机物推断与合成,充分利用反应条件、J的结构特点与分子式进行推断,需要学生熟练掌握官能团的性质与转化,侧重考查学生分析推理能力,难度中等.

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
| A. | 该反应是吸热反应 | |
| B. | 断裂 1 mol A-A 键和 1 mol B-B 键放出 x kJ 的能量 | |
| C. | 断裂 2 mol A-B 键需要吸收 y kJ 的能量 | |
| D. | 2 mol AB 的总能量大于1 mol A2 和 1 mol B2 的总能量 |
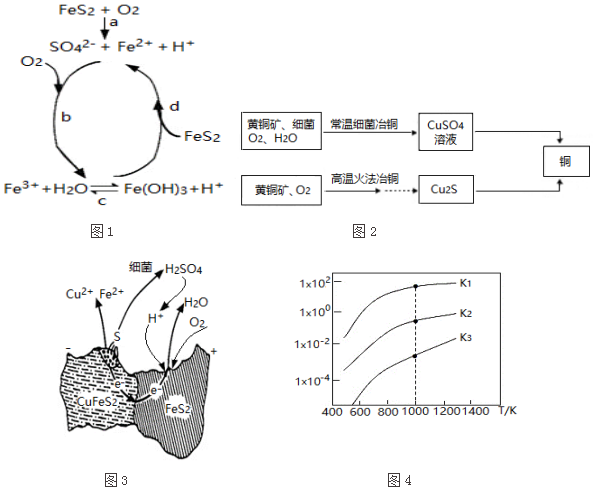
(1)黄铁矿在空气中易被氧化,其反应历程可能为如图1所示的四步:
①a反应中每生成1molFeSO4转移电子的物质的量为7mol.
②d反应的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+.
(2)用黄铜矿常温细菌冶铜和高温火法冶铜的流程如图2所示:
①细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高Cu2+的浸出速率,
其原理如图3所示:
Ⅰ.冶炼过程中,FeS2周边溶液的pH增大(填“增大”、“减小”或“不变”).
Ⅱ.从CuFeS2析出S的反应式是CuFeS2-4e-=Cu2++Fe2++2S.
②火法冶铜时,由Cu2S制得铜的化学方程式是Cu2S+O2 $\frac{\underline{\;高温\;}}{\;}$2Cu+SO2.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见表),其相关反应的平衡常数与温度的关系如图4.
| 相关反应 | 反应热 | 平衡常数 |
| FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| $\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$Fe(s)+H2S(g) | △H2 | K2 |
| FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(举1例).
| A. | 28b/a | B. | 29a/b | C. | ab/28 | D. | 28a/b |
| A的 氢化物 | B的 氢化物 | C的 氢化物 | X的 氧化物 | Y的氢化物 分子构型 | Z原子 |
| 含氢量最高 的有机物 | 水溶液 呈碱性 | 水溶液 呈酸性 | 两性 氧化物 | 正四面体 | 价电子排布为4s2 |
(1)写出对应元素的名称:A碳、B氮、C氟、X铝、Y硅、Z氯
(2)X、Y、Z三种元素原子半径由大到小的顺序是(用元素符号和“>”表示):Ca>Al>Si
(3)写出B的氢化物与C的氢化物反应后生成物的电子式:
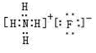 .
.(4)已知C的单质能在水中产生一种常见的氧化性单质,试写出该反应的化学方程式:2F2+2H2O=4HF+O2.
(5)试比较A和Y的最高价氧化物熔点的高低(用具体物质化学式和“>“、“<“或“=“表示:)CO2<SiO2并说明理由CO2为分子晶体,由分子间作用力结合;而SiO2为原子晶体,由共价键结合,共价键强度大于分子间作用力,故SiO2熔点比CO2的熔点高.
| A. | 25℃,Cu(OH)2 在水中的溶度积比其在 Cu(NO3)2 溶液中的大 | |
| B. | 一定温度下,将 0.10 mol/L的氨水加水稀释,溶液中各离子浓度均减小 | |
| C. | H3PO2 属于一元弱酸,则 H3PO2 与过量 NaOH 溶液反应的离子方程式为:H3PO2+3OH?═PO23-+3H2O | |
| D. | 常温下,NaHS 溶液中:c(H+)+c(H2S)═c(S2-)+c(OH-) |
| A. | 分子式为C3H6Cl2的有机物有4种同分异构体 | |
| B. | 包装用材料聚氯乙烯分子中含有碳碳双键 | |
| C. | 苯与液溴混合后加入铁粉发生了加成反应 | |
| D. | 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应 |
 D在周期表的位置:第三周期VIIA族.
D在周期表的位置:第三周期VIIA族.