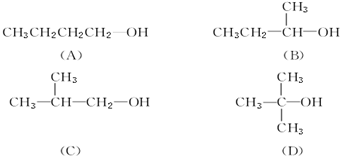题目内容
1.按要求填写(1)官能团“-COOH”的名称是羧基;
(2)甲基的电子式为:
 ;
;(3)有机物
 的系统名称为:3,4,4一三甲基一l一戊炔
的系统名称为:3,4,4一三甲基一l一戊炔(4)某只含C、H、O三种元素的分子模型如图
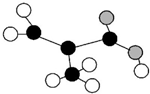 所示(图中球与球之间的连线代表化学键,如单键、双键等).该分子的结构简式为
所示(图中球与球之间的连线代表化学键,如单键、双键等).该分子的结构简式为 .
.
分析 (1)官能团“-COOH”的名称是羧基;
(2)甲基中含有3个碳氢键,碳原子最外层为7个电子,据此写出甲基的电子式;
(3)炔烃命名时,要选含官能团的最长的碳链为主链,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置;
(4)根据图示的该有机物的分子模型判断结构简式.
解答 解:(1)官能团“-COOH”的名称是羧基,故答案为:羧基;
(2)甲基中碳原子最外层为7个电子,甲基的电子式为 ,故答案为:
,故答案为: ;
;
(3)炔烃命名时,要选含官能团的最长的碳链为主链,故主链上有5个碳原子,从离官能团最近的一端给主链上的碳原子编号,故在1号和2号碳原子间有碳碳三键,在3号碳原子上有一个甲基,在4号碳原子上有2个甲基,故名称为3,4,4一三甲基一l一戊炔,故答案为:3,4,4一三甲基一l一戊炔;
(4)由分子模型可知该有机物的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查了有机物的官能团的名称和电子式的书写,题目难度不大,注意掌握常见有机物的命名原则,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
11.下列实验不能作为判断依据的是( )
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的NaOH溶液,判断镁与铝的金属性强弱 | |
| C. | 往硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | 根据HF和HCl的水溶液的酸性强弱判断氟与氯的非金属性的强弱 |
12.下列依据热化学方程式得出的结论正确的是( )
| A. | 若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ/mol,则H2燃烧热为241.8 kJ/mol | |
| B. | 若P4(白磷,s)=4P(红磷,s)△H=-29.2kJ/mol,则红磷比白磷稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.4 kJ/mol,则20.0g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
6.对于达到平衡状态的可逆反应:N2+3H2?2NH3,下列有关叙述正确的是( )
| A. | N2和NH3的质量分数相等 | |
| B. | N2、H2、NH3的浓度之比为1:3:2 | |
| C. | 当断开1mol氮氮三键的同时,断开3mol氢氢键 | |
| D. | 氮气的体积分数保持不变 |
13.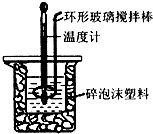 用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
(1)该实验中,量取50mL盐酸或NaOH溶液,需要用到的玻璃仪器除胶头滴管外还要50ml量筒;
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指混合溶液的最高温度;
(4)计算该实验发生中和反应时放出的热量为1344J[中和后生成的溶液的比热容c=4.2J•(g•℃)-1,稀溶液的密度都为1g•cm-3];
(5)若用50mL 0.55mol•L-1的氨水(NH3•H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会偏大(填“偏大”、“偏大”或“不变”),其原因是一水合氨为弱电解质,反应过程中电离需要吸收热量,故放出的热量偏少,△H偏大.
 用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是减少实验过程中的热量损失;
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指混合溶液的最高温度;
(4)计算该实验发生中和反应时放出的热量为1344J[中和后生成的溶液的比热容c=4.2J•(g•℃)-1,稀溶液的密度都为1g•cm-3];
(5)若用50mL 0.55mol•L-1的氨水(NH3•H2O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热△H会偏大(填“偏大”、“偏大”或“不变”),其原因是一水合氨为弱电解质,反应过程中电离需要吸收热量,故放出的热量偏少,△H偏大.
10.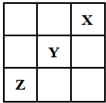 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
 短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )| A. | Y的氢化物稳定性大于Z的氢化物稳定性 | |
| B. | Z一定是活泼的金属元素 | |
| C. | Y的最高价氧化物的水化物是一种强酸 | |
| D. | 1molX的单质可以跟足量水反应,转移的电子为2mol |
11.某课外兴趣小组对H2O2的分解速率做了科学探究,采集的数据见表:
用10mL H2O2制取150mLO2所需的时间(秒)
(1)该小组在设计方案时.考虑了浓度、催化剂、温度等因素对过氧化氢分解速率的影响.
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?
一般加入催化剂,反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
用10mL H2O2制取150mLO2所需的时间(秒)
| 浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 260 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
(2)从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?
一般加入催化剂,反应速率加快(或升高温度反应速率加快,降低温度反应速率减慢;增加反应物浓度,反应速率加快,减小反应物浓度,反应速率减慢).
 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为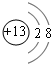 .
.