题目内容
16.下列离子方程式或电离方程式正确的是( )| A. | NaHSO3溶液呈酸性:NaHSO3═Na++H++S032- | |
| B. | 向Na2SiO3溶液中通人少量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 将一小块钠投入稀醋酸中:2Na+2H+═2Na++H2 | |
| D. | 在Na2S203溶液中滴加稀硝酸:2H++S2O32-═S+SO2+H2O |
分析 A.亚硫酸氢根离子为弱酸根离子,部分电离;
B.二氧化碳少量反应生成硅酸和碳酸钠;
C.醋酸为弱酸,保留化学式;
D.向Na2S2O3溶液中加入稀硫酸,反应生成硫单质和二氧化硫气体.
解答 解:A.NaHSO3溶液呈酸性,离子方程式:NaHSO3═Na++HS03-,故A错误;
B.向Na2SiO3溶液中通人少量CO2,离子方程式:SiO32-+CO2+H2O═H2SiO3↓+CO32-,故B正确;
C.将一小块钠投入稀醋酸中,离子方程式:2Na+2CH3COOH═2Na++H2↑+2CH3COO-↑,故C错误;
D.硫代硫酸钠与稀硫酸反应生成硫单质和二氧化硫气体,溶液出现浑浊,生成无色刺激性气味气体,反应的离子方程式为:S2O32-+2H+═SO2↑+S↓+H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写的正误判断,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,本题中注意化学式的拆分、反应物用量对反应的影响.

练习册系列答案
相关题目
7.分子式为C5H10O2并能与NaOH溶液反应的有机构有(不含立体异构)( )
| A. | 11种 | B. | 12种 | C. | 13种 | D. | 14种 |
4.下列有关物质用途的说法不正确的是( )
| A. | 铝制容器可长期存放碱性食物 | B. | 水玻璃浸泡过的木材能防腐 | ||
| C. | 过氧化钠用作呼吸面具中的供氧剂 | D. | 氯气用于农药的生产和药物合成 |
11.短周期主族元素X、Y、Z、W的原子序数依次增大,X在元素周期表中原子半径最小,Y原子在周期表中处于族序数等于周期序数2倍的位置,Z最外层电子数是其核外电子数的3/4,W与Z属于同一主族.下列叙述正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 原子半径:r(Z)<r(Y)<r(W) | |
| C. | W的简单氢化物的热稳定性比Z的强 | |
| D. | Y的最高价氧化物对应的水化物是强酸 |
1.下列有关说法正确的是( )
| A. | 常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度前者比后者大 | |
| B. | 反应Hg(1)+H2SO4(aq)=HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0 | |
| C. | 将纯水加热至较高温度,K变大、pH变小、呈酸性 | |
| D. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时增大氮气的浓度,正逆反应速率均增大,平衡正向移动,氢气的转化率提高 |
5.下列说法正确的是( )
| A. | 实验室用Zn和稀硫酸制H2,为加快反应速率,可向稀硫酸中加入少量Cu粉 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的△H>0 | |
| C. | 在一体积可变的恒温密闭容器中发生反应PCl3(g)+Cl2(g)?PCl5(g),压缩体积,平衡正向移动,K值增大 | |
| D. | 25℃时Ka(HClO)=3.0×10-8,Ka(HCN)=4.9×10-10,若该温度下NaClO溶液与NaCN溶液pH相同,则c(NaClO)<c(NaCN) |
6.将1mol氨气和2mol氧气混和,在800℃铂催化剂作用下充分反应,当恢复到常温常压时,所得的产物是( )
| A. | 二氧化氮与氧气 | B. | 一氧化氮与二氧化氮 | ||
| C. | 硝酸与一氧化氮 | D. | 硝酸与水 |
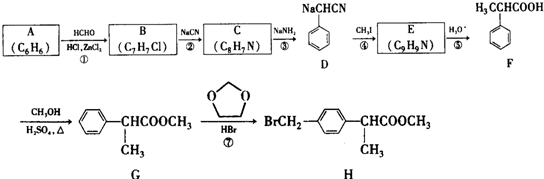
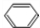 +HCHO+HCl$\stackrel{ZnCl_{2}}{→}$
+HCHO+HCl$\stackrel{ZnCl_{2}}{→}$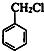 +H2O.
+H2O.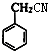 ;E的结构简式为
;E的结构简式为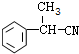 .
. .
.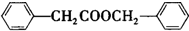 的合成路线
的合成路线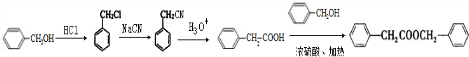 .
.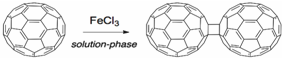

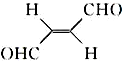 ,下列叙述正确的有AD.
,下列叙述正确的有AD.