题目内容
14. 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
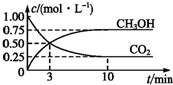
测得CO2和CH3OH(g)的浓度随时间变化如图所示.
(1)反应开始到平衡,H2的平均反应速率v(H2)=0.225mol•L-1•min-1,该反应达平衡时放出热量36.75kJ.
(2)若CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1; CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H2;生成水的质量相等,则△H1>△H2(填“>”、“=”或“<”).
(3)下列描述能说明该反应达到平衡状态的是CD.
A.气体的密度不再变化 B.各组分的浓度相等
C.消耗CO2物质的量与消耗CH3OH物质的量相等 D.CH3OH的体积分数不再变化
(4)下列措施中能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是CE.
A.升高温度 B.恒容充入He使压强增大
C.将H2O(g)从体系中分离 D.使用催化剂 E.缩小容器体积.
分析 (1)图象分析可知甲醇浓度变化,结合化学方程式计算氢气浓度变化,反应速率v=$\frac{△c}{△t}$,反应热与化学计量数成正比,根据热化学方程式计算;
(2)依据盖斯定律结合热化学方程式计算分析焓变大小,注意放热反应的焓变为负值;
(3)根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(4)要使平衡混合物中 $\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,应使平衡向正反应方向移动,根据影响平衡移动的因素来回答判断.
解答 解:(1)图象分析可知甲醇浓度变化为0.75mol/L,化学方程式计算CO2(g)+3H2(g)?CH3OH(g)+H2O(g),氢气浓度变化=3×0.75mol/L=2.25mol/L,
反应开始到平衡,H2的平均反应速率v(H2)=$\frac{2.25mol/L}{10min}$=0.225 mol•L-1•min-1,达到平衡状态消耗甲醇物质的量=0.75mol/L×1L=0.75mol,结合化学方程式定量关系计算反应达到平衡状态放出的热量,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1
1 49.0kJ•mol-1
0.75mol Q=36.75 kJ
故答案为:0.225 mol•L-1•min-1,36.75 kJ;
(2)①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1;
②CO2(g)+3H2(g)?CH3OH(g)+H2O(l)△H2;生成水的质量相等,
盖斯定律计算①-②得到H2O(l)=H2O(g)△H1-△H2,液体水变化为气体水需要吸热,反应焓变大于0,△H1-△H2>0,△H1>△H2,
故答案为:>;
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,反应是气体体积减小的放热反应,
A.反应前后气体体积和质量不变,气体的密度始终不变化,不能说明反应达到平衡状态,故A错误;
B.各组分的浓度相等和起始量、变化量有关,不能说明反应正逆反应速率相同,不能证明反应达到平衡状态,故B错误;
C.消耗CO2物质的量与消耗CH3OH物质的量相等,说明二氧化碳正逆反应速率相同,说明反应达到平衡状态,故C正确;
D.CH3OH的体积分数不再变化是平衡标志,说明反应达到平衡状态,故D正确;
故答案为:CD;
(4)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,反应是气体体积减小的放热反应,要使平衡混合物中 $\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,应使平衡向正反应方向移动,
A.反应是放热反应,反应升高温度 平衡逆向进行,比值减小,故A错误;
B.恒容充入He使压强增大,总压增大,分压不变平衡不变,故B错误;
C.将H2O(g)从体系中分离 平衡正向进行,平衡混合物中 $\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,故C正确;
D.使用催化剂改变反应速率不改变化学平衡,比值不变,故D错误;
E.缩小容器体积,压强增大,平衡正向进行,平衡混合物中 $\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大,故E正确;
故答案为:CE.
点评 本题考查较为综合,涉及热化学方程式计算分析、化学平衡计算、及平衡移动影响因素、平衡标志等问题,题目难度中等,注意根据图象计算各物质的平衡浓度为解答该题的关键.

 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案| A. | 中性溶液AG=0 | |
| B. | 常温下0.1mol/L氢氧化钠溶液的AG=12 | |
| C. | 酸性溶液AG<0 | |
| D. | 常温下0.1mol/L的盐酸溶液的AG=13 |
| A. | 常温常压下,1mol氦气含有的原子数为NA | |
| B. | 常温常压下,8g甲烷中含有的电子数为5NA | |
| C. | 22 g CO2 与标准状况下11.2 L O2含有相同分子数 | |
| D. | 标准状况下,11.2L四氯化碳所含分子数 0.5NA |
| A. | 氟化铵的电子式: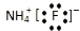 | |
| B. | 原子最外层只有1个电子的元素一定是金属元素 | |
| C. | 离子结构示意图: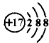 ,可以表示35Cl-,也可以表示37Cl- ,可以表示35Cl-,也可以表示37Cl- | |
| D. | 1mol CH4与1mol NH4+所含质子数相等 |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ||||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(2)②和⑧形成的化合物灼烧时焰色为紫色;
(3)元素⑦的氢化物常温下和元素②的单质反应的离子方程式是2K+2H2O═2K++2OH-+H2↑,用元素⑧的单质制备漂白液的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O;
(4)②③④中形成的简单离子半径由大到小的顺序是K+>Ca2+>Mg2+;
(5)写出①和⑦形成的稳定化合物的电子式
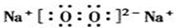 ;
;(6)用电子式表示⑥和⑦形成化合物的形成过程
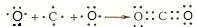 .
. | A. | 透明的溶液中:Al3+、Cu2+、SO42-、NO3- | |
| B. | 通入SO2的溶液中:Fe3+、Ba2+、Cl-、NO3- | |
| C. | 加入铝粉产生H2的溶液中:NH4+、Fe3+、SO42-、NO3- | |
| D. | 常温下,由水电离出的c(H+)=1×10-12mol/L:K+、Ba2+、Cl-、NO3- |


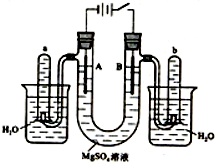 如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色)回答下列问题:
如图是一个用铂丝作电极,电解稀的MgSO4溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色.(指示剂的pH变色范围:6.8~8.0,酸色-红色,碱色-黄色)回答下列问题: