题目内容
15.把4molX气体和 6mol Y气体混合于2L密闭容器中,使它们发生如下反应:X(g)+2Y(g)=3Z(g)+nW(g),5min末生成3molZ,若测知以W的浓度变化来表示的反应速率为0.2mol•(L•min)-1.试计算:(写出计算过程)(1)5min末时X、Y的浓度?
(2)前5min内用X的浓度变化表示的平均反应速率?
(3)化学方程式中n的值.
分析 5min末生成3molZ,v(Z)=$\frac{\frac{3mol}{2L}}{5min}$=0.3mol•(L•min)-1,以W的浓度变化来表示的反应速率为0.2mol•(L•min)-1,由反应速率之比等于化学计量数之比可知,$\frac{0.3}{0.2}=\frac{3}{n}$,解得n=2,则
X(g)+2Y(g)=3Z(g)+2W(g),
开始 4 6 0 0
转化 1 2 3 2
5min 3 4 3 2
结合c=$\frac{n}{V}$、v=$\frac{△c}{△t}$计算.
解答 解:5min末生成3molZ,v(Z)=$\frac{\frac{3mol}{2L}}{5min}$=0.3mol•(L•min)-1,以W的浓度变化来表示的反应速率为0.2mol•(L•min)-1,由反应速率之比等于化学计量数之比可知,$\frac{0.3}{0.2}=\frac{3}{n}$,解得n=2,则
X(g)+2Y(g)=3Z(g)+2W(g),
开始 4 6 0 0
转化 1 2 3 2
5min 3 4 3 2
(1)5min末时X的浓度为$\frac{3mol}{2L}$=1.5mol/L,Y的浓度为$\frac{4mol}{2L}$=2mol/L,
答:5min末时X、Y的浓度分别为1.5mol/L、2mol/L;
(2)前5min内用X的浓度变化表示的平均反应速率为$\frac{\frac{1mol}{2L}}{5min}$=0.1mol•(L•min)-1,
答:X的浓度变化表示的平均反应速率为0.1mol•(L•min)-1;
(3)由上述分析可知化学方程式中n=2,答:n的值为2.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、速率与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

 导学全程练创优训练系列答案
导学全程练创优训练系列答案| A. | 铁是人体健康、植树生长所必须的元素之一,缺铁时可用补充FeSO4的方法补铁 | |
| B. | 在采煤作业中,把炸药和干冰放在一起,既能增强爆炸威力,又能防止火灾 | |
| C. | 氢氧燃料电池已用于航天飞机,燃料电池的能量转化率理论上可达100% | |
| D. | 聚乙烯塑料可用于制作餐具 |
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验.可选用第试剂KSCN溶液、K3[Fe(CN)6]溶液、氯水.
(1)请完成表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 变成血红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6],振荡 | 产生蓝色沉淀 | 存在Fe2+ |
Ⅱ.AgNO3的热稳定性性
用如图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束以后,试管中残留固体为黑色.
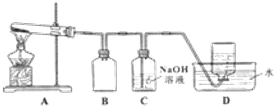
(2)装置B的作用是防倒吸.
(3)经小组讨论并验证该无色气体为O2,其验证方法是用带火星木条靠近瓶口,木条复燃,证明是氧气.
(4)【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水.
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱ.Ag2O;ⅲ.Ag和Ag2O
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,该小组得出的AgNO3固体热分解的产物有Ag、O2、NO2.
| A. | 14g N2和32g O2 | B. | 34g NH3 和4g H2 | ||
| C. | 2LCO2和2LH2O | D. | 11.2LO2和0.5molO2 |
| A. | 钾 | B. | 钙 | C. | 铬 | D. | 铜 |
| A. | 铜 | B. | 氧化铜 | C. | 氢氧化铜 | D. | 硫酸铜 |
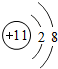 ;
;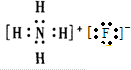 .
.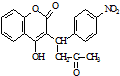
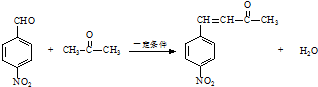
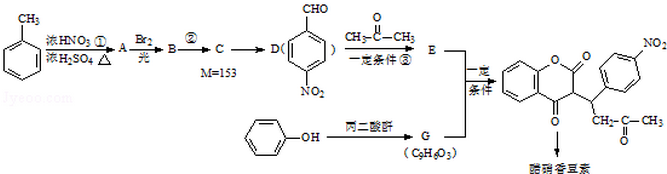 已知:R1-CHO
已知:R1-CHO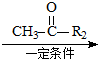 R1-CH=
R1-CH= +H2O
+H2O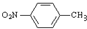 ;反应②的反应类型取代反应.
;反应②的反应类型取代反应.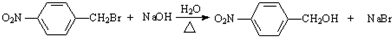 .
. .
.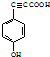 .
.