题目内容
8.火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染和温室效应.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
甲烷直接将NO2还原为N2的热化学方程式为CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol.
(2)脱碳.将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H3
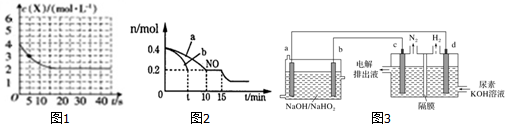
①取五份等体积的CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图1所示,则上述反应的△H3<0(填“>”、“<”或“=”).
②在一恒温恒容密闭容器中充入1molCO2和3molH2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如图2所示.

试回答:0~10min内,氢气的平均反应速率为0.225mol•L-1•min-1;该温度下,反应的平衡常数的值为$\frac{16}{3}$(结果保留一位小数);第10min后,向该容器中再充入1molCO2和3molH2,则再次达到平衡时CH3OH(g)的体积分数变大(填“变大”、“减少”、“不变”).
(3)脱硫.
①某种脱硫工艺中将废弃经处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液.使溶液的pH=7,则溶液中:c(Na+)+c(H+)<c(NO3-)+c(OH-)(填“>”、“<”“=”).
②如图3电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-.物质A的化学式为H2SO4,阴极的电极反应式是NO+5e-+6H+=NH4++H2O.
分析 (1)根据盖斯定律和热化学方程式的意义和书写方法,(①+②)×$\frac{1}{2}$得到热化学方程式;
(2)①图象分析,甲醇含量随温度变化的曲线特征,开始反应进行,平衡后,升温平衡逆向进行,根据温度对化学平衡移动的影响知识来回答;
②三段式来计算平衡浓度,根据化学反应速率v=$\frac{△c}{△t}$以及平衡常数的表达式计算,0~10min内,二氧化碳的平均反应速率=$\frac{1.0mol/L-0.25mol/L}{10min}$=0.075mol/(L•min),所以氢气的反应速率是3×0.075mol/(L•min)=0.225mol/(L•min),
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
初始浓度:1 3 0 0
变化浓度:0.75 2.25 0.75 0.75
平衡浓度:0.25 0.75 0.75 0.75
平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$;并根据压强对化学平衡移动的影响知识来回答;
(3)①溶液中铵根离子水解显示酸性,硝酸铵溶液中滴加适量的NaOH溶液溶液的pH=7,则氢离子和氢氧根离子浓度相等,根据电荷守恒来计算;
②电解装罝可将雾霾中的NO、SO2分别转化为NH4+和SO42-,则电解方程式为5SO2+2NO+8H2O$\frac{\underline{\;电解\;}}{\;}$(NH4)2SO4+4H2SO4,根据电解方程式结合电解原理分析
解答 解:(1)①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
由盖斯定律(①+②)×$\frac{1}{2}$得到热化学方程式为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=$\frac{1}{2}$(-574kJ•mol-1-1160kJ•mol-1)=-867 kJ/mol,
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ/mol;
(2)①根据图象分析知道:温度升高,甲醇的体积分数φ(CH3OH)减小,平衡逆向移动,所以反应是放热的,即△H<0,
故答案为:<;
②0~10min内,二氧化碳的平均反应速率=$\frac{1.0mol/L-0.25mol/L}{10min}$=0.075mol/(L•min),所以氢气的反应速率是3×0.075mol/(L•min)=0.225mol/(L•min),
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
初始浓度:1 3 0 0
变化浓度:0.75 2.25 0.75 0.75
平衡浓度:0.25 0.75 0.75 0.75
所以平衡常数K=$\frac{0.7{5}^{2}}{0.25×0.7{5}^{3}}$=$\frac{16}{3}$向该容器中再充入1mol CO2和3mol H2,会使得压强增大,平衡正向移动,所以再次达到平衡时CH3OH(g)的体积分数变大,
故答案为:0.225;$\frac{16}{3}$;变大;
(3)①硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,溶液中存在电荷守恒:c(Na+)+c(H+)+c(NH4+)=c(NO3-)+c(OH-),则c(Na+)+c(H+)<c(NO3-)+c(OH-),
故答案为:<;
②电解装罝可将雾霾中的NO、SO2分别转化为NH4+和SO42-,则电解方程式为5SO2+2NO+8H2O$\frac{\underline{\;电解\;}}{\;}$(NH4)2SO4+4H2SO4,由电解方程式可知,物质A为硫酸,其的化学式H2SO4; 电解时,阳极上二氧化硫失电子生成硫酸根离子,则阳极的电极反应式是SO2+2H2O-2 e-═SO42-+4H+,阴极反应式为:NO+5e-+6H+=NH4++H2O,
故答案为:H2SO4;NO+5e-+6H+=NH4++H2O.
点评 本题考查较为综合,涉及化学平衡计算、反应热与焓变、电解原理、化学平衡的影响等知识,题目难度较大,明确化学平衡及其影响为解答关键,注意掌握盖斯定律的内容及应用方法.

| A. | Al(OH)3$\stackrel{电解}{→}$ Al$→_{高温}^{Fe_{2}O_{3}}$ Fe | |
| B. | S$\stackrel{O_{2}/点燃}{→}$ SO3$\stackrel{H_{2}O}{→}$ H2SO4 | |
| C. | Cu2(OH)2CO3$\stackrel{盐酸}{→}$CuCl2(aq)$\stackrel{电解}{→}$ Cu | |
| D. | Fe2O3$\stackrel{HCl(aq)}{→}$ FeCl3(aq)$\stackrel{△}{→}$ 无水FeCl3 |
| A. | 0 | B. | 10 | C. | 2 | D. | 8 |
| A. | 治疗疟疾的青蒿素(如图),分子式为C15H20O5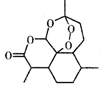 | |
| B. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| C. | 对三联苯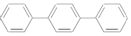 分子中至少有16个原子共平面 分子中至少有16个原子共平面 | |
| D. | 油脂和乙烯在一定条件下都能与水反应,且反应类型相同 |
| A. | 简单离子半径:a<c<d<e | |
| B. | 气态氢化物的稳定性e<b<c | |
| C. | 最高价氧化物的水化物酸性b>e | |
| D. | c和d形成的化合物溶于水后溶液呈碱性 |
(1)若实验中大约要使用475mLNaOH溶液,至少需要称量NaOH固体2.0g.
(2)从如图中选择称量NaOH固体所需要的仪器是(填字母)abe.
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
①称量读数时,左盘高,右盘低
②所用的砝码生锈
③溶液转移到容量瓶后,未进行洗涤操作
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
⑦定容后摇匀,发现液面降低,又补加少量水,重新达到刻度实验室欲配制
⑧用量筒量取一定量浓硫酸配制稀硫酸,转移到烧杯后,用少量水洗涤量筒.