题目内容
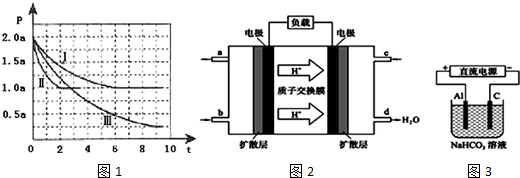
13.在容积不变的密闭容器中存在如下可逆反应aA(g)+bB(g)?cC(g)+dD(s)△H=Q kJ•mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示.据图分析,以下说法正确的是( )
| A. | T1<T2,Q>0 | |
| B. | 增大压强,B的转化率减小 | |
| C. | 当混合气体的密度不再变化,反应达平衡状态 | |
| D. | a+b<c+d |
分析 A.根据“先拐先平数值大”知,T1<T2,升高温度平衡向吸热方向移动;
B.增大压强正逆反应速率都增大,但正反应速率大于逆反应速率,平衡正向移动;
C.反应前后气体总质量减小,容器体积不变,则密度减小;
D.增大压强平衡向气体体积减小的方向移动.
解答 解:A.根据“先拐先平数值大”知,T1<T2,升高温度平衡向吸热方向移动,升高温度产物含量减小,说明平衡逆向移动,则正反应是放热反应,Q<0,故A错误;
B.增大压强正逆反应速率都增大,但正反应速率大于逆反应速率,平衡正向移动,B的转化率增大,故B错误;
C.反应前后气体总质量减小,容器体积不变,则密度减小,但容器内气体密度不变时正逆反应速率相等,反应达到平衡状态,故C正确;
D.增大压强平衡向气体体积减小的方向移动,增大压强平衡正向移动,则a+b>c,故D错误;
故选C.
点评 本题考查图象分析,为高频考点,明确温度、压强对化学平衡移动影响原理是解本题关键,侧重考查学生分析判断能力,明确“先拐先平数值大”是解本题关键,难点是分析乙图,题目难度中等.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
8.乙酸乙酯在KOH溶液催化下水解得到的产物是( )
| A. | 乙酸和乙醇 | B. | 甲酸和乙醇 | C. | 乙酸钾和乙醇 | D. | 乙酸和甲醇 |
18. CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol
CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol
反应过程中测定的部分数据如表:
(1)比较各时段平均速率v(COCl2):v(0-1)> v(0-2);v(0-2)> v(1-2) (填“>”、“=”或“<”).
(2)在2min~4min间,v(Cl2)正=v(Cl2)逆 (填“>”、“=”或“<”),该温度下K=5
(3)已知X、L可分别代表温度或压强,如图表示L一定时,CO的砖化率随X的变化关系.
X代表的物理量是温度;a<0 (填“>”,“=”,“<”),依据是因为X增大时,CO的平衡转化率降低,平衡逆向移动.
 CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol
CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)?COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如表:
| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
(2)在2min~4min间,v(Cl2)正=v(Cl2)逆 (填“>”、“=”或“<”),该温度下K=5
(3)已知X、L可分别代表温度或压强,如图表示L一定时,CO的砖化率随X的变化关系.
X代表的物理量是温度;a<0 (填“>”,“=”,“<”),依据是因为X增大时,CO的平衡转化率降低,平衡逆向移动.
5.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(CO32-) | |
| B. | 20ml0.1mol/LCH3COONa溶液与10ml0.1mol/LHCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
2.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L H2O中含有氢原子数目为2NA | |
| B. | 17 g NH3所含质子数为10NA | |
| C. | 0.1mol Cu(NO3)2中含有的离子数目为0.2NA | |
| D. | 28g N2 体积为22.4L |

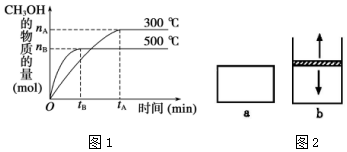 一定条件下,在体积为 3L 的密闭容器中反应 CO(g)+2H2(g)?CH3OH(g)△H=akJ•mol-1,△S=b J•mol-1•K-1(a、b 均为正数),达到化学平衡状态.
一定条件下,在体积为 3L 的密闭容器中反应 CO(g)+2H2(g)?CH3OH(g)△H=akJ•mol-1,△S=b J•mol-1•K-1(a、b 均为正数),达到化学平衡状态.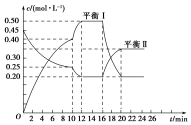 向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)?yC(g)△H<0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示.请回答下列问题:
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)?yC(g)△H<0在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示.请回答下列问题: