题目内容
通过下列实验现象的分析,对实验事实的解释正确的是( )
| A、向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,说明BaCl2有酸性 |
| B、H2S能与CuSO4溶液反应生成H2SO4,说明氢硫酸的酸性比硫酸强 |
| C、用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色,说明浓氨水呈碱性 |
| D、常温下,将铝片放入浓硫酸中,无明显现象,说明铝不与冷的浓硫酸发应 |
考点:浓硫酸的性质,氨的化学性质
专题:
分析:A、二者反应生成中性的氯化钠;
B、H2S通入CuSO4溶液中生成黑色沉淀为CuS,并生成硫酸;
C、试纸变蓝色,说明浓氨水呈碱性;
D、铝与冷的浓硫酸发生钝化现象.
B、H2S通入CuSO4溶液中生成黑色沉淀为CuS,并生成硫酸;
C、试纸变蓝色,说明浓氨水呈碱性;
D、铝与冷的浓硫酸发生钝化现象.
解答:
解:A、Na2CO3+BaCl2=BaCO3↓+2NaCl,碳酸钠溶液呈碱性、氯化钠溶液呈中性,所以溶液会褪色,故A错误;
B、H2S通入CuSO4溶液中生成黑色沉淀为CuS,并生成硫酸,由化学平衡移动可知,生成CuS沉淀使反应能发生,但不能利用此反应说明强酸制取弱酸,故B错误;
C、试纸变蓝色,说明浓氨水呈碱性,故C正确;
D、铝与冷的浓硫酸发生钝化现象,而不是不反应,故D错误;
故选C.
B、H2S通入CuSO4溶液中生成黑色沉淀为CuS,并生成硫酸,由化学平衡移动可知,生成CuS沉淀使反应能发生,但不能利用此反应说明强酸制取弱酸,故B错误;
C、试纸变蓝色,说明浓氨水呈碱性,故C正确;
D、铝与冷的浓硫酸发生钝化现象,而不是不反应,故D错误;
故选C.
点评:本题考查了化学实验方案评价,涉及离子反应、酸性强弱判断、钝化现象等知识点,明确物质的性质是解本题关键,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列事实得出的结论正确的是( )
| A、可用加热法除去氯化钠固体中的氯化铵杂质 |
| B、只用铜片不能鉴别浓硝酸和稀硝酸 |
| C、常温下,Al和浓硫酸钝化说明Al和浓硫酸在常温下不反应 |
| D、SO2通入氯化钡溶液无现象,若再通入NH3或NO2气体则都会产生BaSO4的白色沉淀 |
25℃时pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得混合液的pH=11,则NaOH溶液与H2SO4溶液的体积比是( )
| A、1:9 | B、1:11 |
| C、9:1 | D、11:1 |
ICl能发生下列变化,其中变化时会破坏化学键的是( )
| A、升华 |
| B、熔化 |
| C、溶于CCl4 |
| D、受热分解 |
天然碱的化学式表示为2Na2CO3?NaHCO3?2H2O,取少量该物质溶于水得到稀溶液,在溶液中逐滴加入稀盐酸.下列离子方程式与事实不相符的是( )
| A、HCO3-+CO32-+3H+→2H2O+2CO2↑ |
| B、2HCO3-+CO32-+4H+→3H2O+3CO2↑ |
| C、CO32-+H+→HCO3- |
| D、HCO3-+3CO32-+7H+→4H2O+4CO2↑ |
关于元素周期律的叙述不正确的是( )
| A、同周期元素,从左到右电负性依次增大 |
| B、主族元素的最高化合价都等于最外层电子数(O、F除外) |
| C、同主族元素,从上到下,原子半径依次增大 |
| D、金属元素的正化合价越高,其对应的氢氧化物的碱性越强 |
 .
.
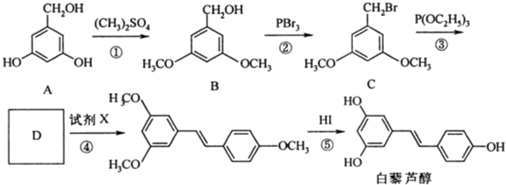
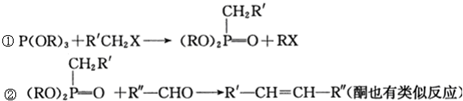
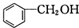 和P(OC2H5)3为原料,选择适当的无机试剂和催化剂,通过合理的途径合成
和P(OC2H5)3为原料,选择适当的无机试剂和催化剂,通过合理的途径合成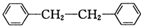 .请补全下列合成路线(含条件、试剂和主要产物的结构简式).
.请补全下列合成路线(含条件、试剂和主要产物的结构简式).