题目内容
甲醇来源丰富,价格低廉,是一种重要的化工原料,有着非常重要、广泛的用途.工业上通常用水煤气在恒容、催化剂和加热的条件下生产甲醇,其热化学方程式为:2H2(g)+CO(g)?CH3OH(g)△H=-90.8kJ/mol.
(1)该反应的平衡常数表达式为:K= ,如升高温度,K值将 (填:增大、减小或不变).
(2)以下各项不能说明该反应达到平衡状态的是 .
A、混合气体的密度保持不变
B、甲醇的质量分数保持不变
C、CO的浓度保持不变
D、2v逆(H2)=v正(CH3OH)
(3)在2100C、2400C和2700C三种不同温度、2L恒容密闭容器中研究合成甲醇的规律.
图1是上述三种温度下不同的H2和C0的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是 .由起始达到 a 点所需时间为 5min,则 H2的反应速率 mol/(L?min) .
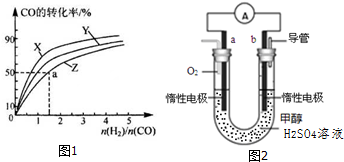
(4)某兴趣小组设计了如图2所示的甲醇燃料电池装置.
①该电池工作时,正极是 极(填“a”或“b”);
②该电池负极反应的离子方程式为 .
(1)该反应的平衡常数表达式为:K=
(2)以下各项不能说明该反应达到平衡状态的是
A、混合气体的密度保持不变
B、甲醇的质量分数保持不变
C、CO的浓度保持不变
D、2v逆(H2)=v正(CH3OH)
(3)在2100C、2400C和2700C三种不同温度、2L恒容密闭容器中研究合成甲醇的规律.
图1是上述三种温度下不同的H2和C0的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是

(4)某兴趣小组设计了如图2所示的甲醇燃料电池装置.
①该电池工作时,正极是
②该电池负极反应的离子方程式为
考点:化学平衡常数的含义,原电池和电解池的工作原理,化学平衡状态的判断,化学平衡的计算
专题:
分析:(1)平衡常数等于生成物与反应物的浓度幂的之积,正反应为放热反应,升高温度平衡逆向移动;
(2)反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,以此判断;
(3)正反应放热,则升高温度CO的转化率降低;a 点CO的转化率为50%,以此计算氢气的物质的量浓度的变化,进而计算反应速率;
(4)燃料电池中通入氧气的为正极,通入甲醇的为负极,负极发生氧化反应.
(2)反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,以此判断;
(3)正反应放热,则升高温度CO的转化率降低;a 点CO的转化率为50%,以此计算氢气的物质的量浓度的变化,进而计算反应速率;
(4)燃料电池中通入氧气的为正极,通入甲醇的为负极,负极发生氧化反应.
解答:
解:(1)平衡常数等于生成物与反应物的浓度幂的之积,为
,正反应为放热反应,升高温度平衡逆向移动,则平衡常数减小,
故答案为:K=
;减小;
(2)A、因容器体积不变,则无论受否达到平衡状态,则混合气体的密度保持不变,不能用于判断是否达到平衡,故A错误;
B、甲醇的质量分数保持不变,可说明达到平衡状态,故B正确;
C、CO的浓度保持不变,可说明达到平衡状态,故C正确;
D、2v逆(H2)=v正(CH3OH),正逆反应速率不等,没有达到平衡状态,姑姑D错误.
故答案为:AD;
(3)该反应为放热反应,温度越高CO的转化率越小,所以曲线X为210℃,由图象可知曲线Z为270℃,
a 点CO的转化率为50%,则△n(CO)=0.5mol,△n(H2)=1mol,
H2的反应速率为
=0.1mol/(L?min),
故答案为:270℃; 0.1mol/(L?min);
(4)①燃料电池中通入氧气的为正极,发生还原反应,故答案为:a;
②甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:CH3OH-6e-+H2O=CO2↑+6H+,
故答案为:CH3OH-6e-+H2O=CO2↑+6H+.
| c(CH3OH) |
| c(CO)c2(H2) |
故答案为:K=
| c(CH3OH) |
| c(CO)c2(H2) |
(2)A、因容器体积不变,则无论受否达到平衡状态,则混合气体的密度保持不变,不能用于判断是否达到平衡,故A错误;
B、甲醇的质量分数保持不变,可说明达到平衡状态,故B正确;
C、CO的浓度保持不变,可说明达到平衡状态,故C正确;
D、2v逆(H2)=v正(CH3OH),正逆反应速率不等,没有达到平衡状态,姑姑D错误.
故答案为:AD;
(3)该反应为放热反应,温度越高CO的转化率越小,所以曲线X为210℃,由图象可知曲线Z为270℃,
a 点CO的转化率为50%,则△n(CO)=0.5mol,△n(H2)=1mol,
H2的反应速率为
| ||
| 5min |
故答案为:270℃; 0.1mol/(L?min);
(4)①燃料电池中通入氧气的为正极,发生还原反应,故答案为:a;
②甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:CH3OH-6e-+H2O=CO2↑+6H+,
故答案为:CH3OH-6e-+H2O=CO2↑+6H+.
点评:本题综合性较大,涉及化学平衡常数、化学平衡影响因素以及电化学知识等,为高考常见题型,侧重于学生的分析、计算能力的考查,难度较大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
下列关于Na2CO3和NaHCO3性质的说法错误的是( )
| A、热稳定性:NaHCO3<Na2CO3 |
| B、与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3 |
| C、相同温度时,在水中的溶解性:NaHCO3<Na2CO3 |
| D、等物质的量浓度溶液的pH:NaHCO3<Na2CO3 |
常温下某强酸溶液和某强碱溶液的pH之和为13,将这种酸和这种碱按一定比例混合,溶液恰好呈中性,混合时酸和碱的体积之比是( )
| A、10:1 | B、1:10 |
| C、1:1 | D、1:2 |
点燃一根蜡烛,将火焰上方罩一只冷的干燥的烧杯,在烧杯内壁出现水珠,由此得出石蜡的组成中一定含有( )
| A、碳元素 | B、氢元素 |
| C、氧元素 | D、氢、氧元素 |


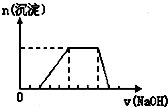 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是
