题目内容
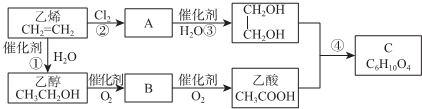
5.高效低毒杀虫剂氯菊酯(I)可通过下列合成路线制备:A(C4H8)+B(C2HOCl3)$→_{①}^{AlCl_{3}}$
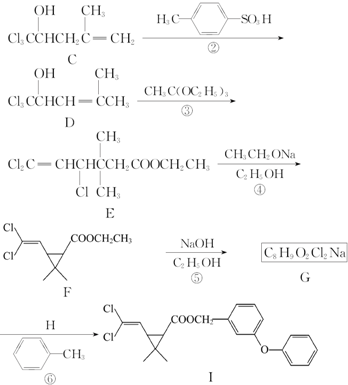
化合物A能使溴的四氯化碳溶液褪色.
(1)A的名称2-甲基-1-丙烯,B的结构简式Cl3C-CHO.
(2)上述合成路线中,原子利用率为100%的反应有①②(填写反应标号).
(3)写出I中含有的两种官能团名称:氯原子、碳碳双键、酯基、醚键(任写两种).
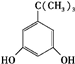
(4)J比F少两个氯,满足下列条件的J的同分异构体有3种,写出一种J的结构简式:
 、
、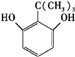 、
、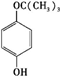 任意一种.
任意一种.①分子中含有苯环,②能与FeCl3溶液反应显紫色,
③核磁共振氢谱有4个吸收峰,且峰面积之比是9:2:2:1
(5)请设计合理的方案以
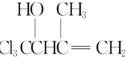 为原料合成
为原料合成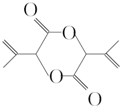 (用合成路线流程图表示,并注明反应条件).
(用合成路线流程图表示,并注明反应条件).提示:①合成过程中无机试剂任选;②两个或两个以上羟基同时连在同一碳原子上的结构是不稳定的,它将发生脱水反应,如CH3CH(OH)2→CH3CHO+H2O;③合成路线流程图示例如下:
CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$BrH2C-CH2Br.
分析 (1)化合物A能使溴的四氯化碳溶液褪色,结合C的结构简式以及A、B分子式可知,A为(CH3)2C=CH2,B为Cl3C-CHO;
(2)反应①为加成反应,反应②中C、D互为同分异构体,因此这两个反应原子利用率为100%;
(3)I中含有氯原子、碳碳双键、酯基、醚键四种官能团;
(4)根据F的结构,则J的分子式为C10H14O2,分子中含有4个不饱和度,则分子中除含有一个苯环外,其余碳原子均为饱和碳原子.根据题意,J分子中含有4种氢原子,且个数比为9:2:2:1,其中有9个氢原子为一种,则可能含有3个相同的甲基或-C(CH3)3,分子中还含有酚羟基;
(5)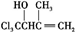 水解后酸化可生成
水解后酸化可生成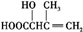 ,发生酯化反应可得目标产物.
,发生酯化反应可得目标产物.
解答 解:(1)化合物A能使溴的四氯化碳溶液褪色,结合C的结构简式以及A、B分子式可知,A为(CH3)2C=CH2,B为Cl3C-CHO,A的名称为:2-甲基-1-丙烯,
故答案为:2-甲基-1-丙烯;Cl3C-CHO;
(2)反应①为加成反应,反应②中C、D互为同分异构体,因此这两个反应原子利用率为100%,
故答案为:①②;
(3)I中含有氯原子、碳碳双键、酯基、醚键四种官能团,
故答案为:氯原子、碳碳双键、酯基、醚键(任写两种);
(4)根据F的结构,则J的分子式为C10H14O2,分子中含有4个不饱和度,则分子中除含有一个苯环外,其余碳原子均为饱和碳原子.根据题意,J分子中含有4种氢原子,且个数比为9:2:2:1,其中有9个氢原子为一种,则可能含有3个相同的甲基或-C(CH3)3,分子中还含有酚羟基,则满足题意的J结构可能为 、
、 、
、 ,共有3种,
,共有3种,
故答案为:3; 、
、 、
、 任意一种;
任意一种;
(5)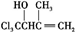 水解后酸化可生成
水解后酸化可生成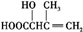 ,发生酯化反应可得目标产物,合成路线流程图为:
,发生酯化反应可得目标产物,合成路线流程图为: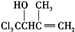 $→_{△}^{NaOH、H_{2}O}$
$→_{△}^{NaOH、H_{2}O}$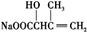 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$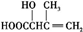 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$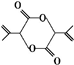 ,
,
故答案为: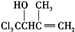 $→_{△}^{NaOH、H_{2}O}$
$→_{△}^{NaOH、H_{2}O}$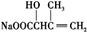 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$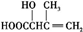 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ .
.
点评 本题考查有机物推断与合成、官能团结构与性质、同分异构体书写、有机反应方程式书写等,是对有机化学的综合可知,侧重考查学生分析推理、知识迁移应用,难点中等.

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案| A. | 合成氨生产中将NH3液化分离,虽可提高N2、H2的转化率但减小了反应速率 | |
| B. | 硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 | |
| D. | 侯氏制碱法是将氨气和二氧化碳先后通入饱和氯化钠溶液中,制得碳酸氢钠固体,再在高温下灼烧,转化为碳酸钠固体 |
| A. | HOCH2CH2CH2OH | B. | CH3OH | C. | CH3CH2OH | D. | HOCH2CH2OH |
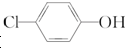 )的废水可以利用微生物电池除去,其原理如图所示,下列说法错误的是( )
)的废水可以利用微生物电池除去,其原理如图所示,下列说法错误的是( )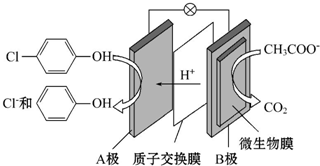
| A. | 该装置能将化学能转化为电能 | |
| B. | A极为正极 | |
| C. | B极上发生氧化反应 | |
| D. | 每有1 mol CH3COO-被氧化,就有8 mol电子通过整个电路 |
| A. | 该锂电池在放电过程中,Li+从正极区向负极区迁移 | |
| B. | 电解质溶液中混入水,对电池反应无影响 | |
| C. | 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 | |
| D. | 电池工作过程中,金属锂提供的电子与正极生成硫的物质的量之比为4:1 |
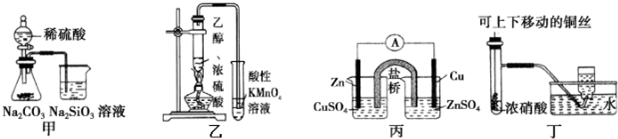
| A. | 图甲证明非金属性强弱:S>C>Si | |
| B. | 装置乙可用于检验有乙烯生成 | |
| C. | 图丙构成铜锌原电池,产生持续稳定的电流 | |
| D. | 图丁可制备并收集NO2气体 |
| A. | 1.8g重水(D2O)中含NA个中子 | |
| B. | 8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| C. | 0.5 mol NH4HSO4晶体中,含有H+数目约为0.5 NA | |
| D. | 标准状况下,密度为d g/L的某气体纯净物一个分子的质量为$\frac{22.4d}{{N}_{A}}$g |