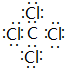题目内容
7.A、B、C、D四种可溶的化合物(所含离子各不相同),分别由阳离子Na+、Mg2+、Al3+、Ba2+和阴离子OH-、Cl-、SO42-、CO32-两两组合而成.为了确定这四种化合物的成份,某同学进行了如下实验操作:①将四种化合物各取适量配成溶液,分别装入四支试管.
②取A溶液分别滴入另外三种溶液中,记录实验现象如下:
B溶液$\stackrel{滴入A溶液}{→}$白色沉淀$\stackrel{再加A溶液}{→}$沉淀不溶解,
C溶液$\stackrel{滴入A溶液}{→}$白色沉淀$\stackrel{再加A溶液}{→}$沉淀不溶解,
D溶液$\stackrel{滴入A溶液}{→}$白色沉淀$\stackrel{再加A溶液}{→}$沉淀部分溶解.
③向B溶液中滴入D溶液,无明显实验现象.
请回答下列问题:
(1)请写出下列物质的化学式:BMgCl2 CNa2CO3
(2)上述②的第三次实验,再加入A,沉淀部分溶解的离子方程式为Al(OH)3+OH-═AlO2-+2H2O
(3)写出A与D溶液混合时,其中D中溶质的阳离子恰好完全沉淀的离子反应方程式2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓.
分析 分析4种阳离子和4种阴离子之间的关系可知CO32-只能与Na+结合成Na2CO3,而OH-只能与Ba2+结合成Ba(OH)2.对照实验②可知A为Ba(OH)2,生成的白色沉淀分别是BaCO3、Mg(OH)2、Al(OH)3、BaSO4,D溶液中生成的白色淀淀再加Ba(OH)2溶液后沉淀部分溶解,说明D是Al2(SO4)3,溶液B可能是Na2CO3或MgCl2.根据实验③可确定溶液B是MgCl2,则C是Na2CO3;(2)中沉淀部分溶解是氢氧化铝溶于强碱性质;(3)中CO32-与Al3+发生双水解反应生成气体和沉淀;
根据分析可知A为Ba(OH)2,B为MgCl2,C为Na2CO3,D为Al2(SO4)3,据此进行解答.
解答 解:分析4种阳离子和4种阴离子之间的关系可知CO32-只能与Na+结合成Na2CO3,而OH-只能与Ba2+结合成Ba(OH)2.对照实验②可知A为Ba(OH)2,生成的白色沉淀分别是BaCO3、Mg(OH)2、Al(OH)3、BaSO4,D溶液中生成的白色淀淀再加Ba(OH)2溶液后沉淀部分溶解,说明D是Al2(SO4)3.溶液B可能是Na2CO3或MgCl2.根据实验③可确定溶液B是MgCl2,则C是Na2CO3,
(1)根据分析可知:A为Ba(OH)2,B为MgCl2,C为Na2CO3,D为Al2(SO4)3,
故答案为:MgCl2;Na2CO3;
(2)②的第三次实验中沉淀部分溶解是氢氧化铝溶于强碱性质,离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O;
(3)A为Ba(OH)2,D为Al2(SO4)3,A与D溶液混合时,其中D中溶质的阳离子恰好完全沉淀的离子反应方程式为:2Al3++3SO42-+3Ba2++6OH-=2 Al(OH)3↓+3BaSO4↓,
故答案为:2Al3++3SO42-+3Ba2++6OH-=2 Al(OH)3↓+3BaSO4↓.
点评 本题考查无机物的推断,属于离子共存实验题目,题目难度中等,明确常见离子的性质为解答关键,对学生的逻辑推理有一定的要求,需要学生具有扎实的基础,试题培养了学生的灵活应用能力.

 阅读快车系列答案
阅读快车系列答案| A. | pH=1的溶液:Ag+、Al3+、Cl-、SO42- | |
| B. | 能使酚酞试液变红的溶液:Na+、K+、HCO3-、S2- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液:NH4+、Cu2+、NO3-、Cl- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液:K+、Fe2+、SO42-、NO3- |
| 实 验 事 实 | 结 论 | |
| ① | Cl2的水溶液可以导电 | Cl2是电解质 |
| ② | 将烧红的铁片插入水中生成氢气 | 还原性:Fe>H2 |
| ③ | 向久置空气的漂白粉中加盐酸有CO2气体产生 | 酸性:H2CO3>HClO |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定含有NH4+ |
| A. | ③④⑤ | B. | ②③⑤ | C. | ①②③ | D. | 全部 |
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)═c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)═2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2溶液:c(Na+)+c(Ca2+)═c(CH3COO-)+c(OH-)+c(Cl-) |
| A. | 原生铜的硫化物具有还原性 | |
| B. | 常温时ZnS、PbS、CuS都难溶于水,CuSO4可溶于水 | |
| C. | 铜蓝的形成过程是:ZnS(S)+Cu2+?CuS(S)+Zn2+ | |
| D. | 硝酸型酸雨不利于铜蓝的形成:CuS+2H+═Cu2++H2S↑ |

| A. | 铜片表面发生氧化反应 | B. | 电子从铜片流向锌片 | ||
| C. | 电流从锌片流向铜片 | D. | 锌片为负极铜片为正极 |
| A. | 增大c(CH3COOH),b增大 | B. | 加水稀释,b减小 | ||
| C. | b的大小只与温度有关 | D. | 以上说法均不对 |
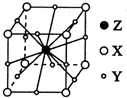 X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂,化合物ZW2的晶体为离子晶体. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.
X、Y、Z、W为短周期元素且原子序数依次增大.X的一种气态氢化物m可用来焊接或切割金属,且该分子所有原子在一条直线上.Y2-的M能层的原子轨道为全空状态.Z的单质用作铝热反应的引燃剂,化合物ZW2的晶体为离子晶体. W与X形成的化合物是一种常见的有机溶剂n.A为第四周期元素,其基态原子含有6个未成对电子.