题目内容
9.某些化学反应可用右式表示:A+B→C+D+H2O (未配平,反应条件略去).请回答下列问题;(1)若C为氯化钠,D是能使澄清石灰水变浑浊的无味气体,若A为无氧酸,则B可能是NaHCO3或Na2CO3(填化学式).
(2)若A为某浓溶液,C、D均为气体,其中C可以使品红褪色,则A为浓硫酸,C为CO2.
(3)若A、C、D均含有氯元素,且A中氯元素的化合价介于C和D之间,B为强碱,写出该化学反应方程式:Cl2+2OH-=Cl-+ClO-+H2O.
(4)若A为Al,D为NO,反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O.
(5)若A为具有磁性的黑色固体,B为无氧酸,C和D含有的元素种类相同,写出该反应的化学方程式:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O.
分析 (1)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,若A为无氧酸,可为NaHCO3或Na2CO3与盐酸的反应;
(2)若A为某浓溶液,C、D均为气体,其中C可以使品红褪色即为SO2,可为浓硫酸与碳的反应;
(3)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应;
(4)若A为Al,D为NO,可为铝与稀硝酸反应生成硝酸铝、NO和H2O;
(5)若A为具有磁性的黑色固体即Fe3O4,B为无氧酸即HCl,C和D含有的元素种类相同,可为Fe3O4与HCl反应生成氯化铁、氯化亚铁和水.
解答 解:(1)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,应为CO2,若A为无氧酸,可为NaHCO3或Na2CO3与盐酸的反应,则A是HCl,B可能是NaHCO3或Na2CO3,故答案为:NaHCO3;Na2CO3;
(3)若A为某浓溶液,C、D均为气体,其中C可以使品红褪色即为SO2,可为浓硫酸与碳反应生成二氧化硫、二氧化碳和水,则A为浓硫酸,C为CO2,故答案为:浓硫酸;CO2;
(3)若A、C、D均含有氯元素,且A的化合价介于C与D之间,常见反应为氯气和氢氧化钠的反应,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(4)若A为Al,D为NO,可为铝与稀硝酸反应生成硝酸铝、NO和H2O,反应的化学方程式为Al+4HNO3=Al(NO3)3+NO↑+2H2O,故答案为:Al+4HNO3=Al(NO3)3+NO↑+2H2O;
(5)若A为具有磁性的黑色固体即Fe3O4,B为无氧酸即HCl,C和D含有的元素种类相同,可为Fe3O4与HCl反应生成氯化铁、氯化亚铁和水,反应的化学方程式为Fe3O4+8HCl=2FeCl3+FeCl2+4H2O,
故答案为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O.
点评 本题综合考查无机物的推断,全面考查学生的分析能力和元素化合物知识的综合运用,为高频考点,注意相关基础知识的积累,牢固把握元素化合物知识为解答该题的关键,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 苯与浓溴水在铁做催化剂的条件下制备溴苯 | |
| B. | H2N-CH2-COOH, , ,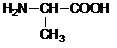 三种氨基酸脱水缩合,最多生成6种二肽 三种氨基酸脱水缩合,最多生成6种二肽 | |
| C. |  与氢氧化钠醇溶液共热,可得2种产物 与氢氧化钠醇溶液共热,可得2种产物 | |
| D. | 分子式为C5H12O的有机物,能与Na反应放出氢气的结构有8种 |
| A. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| B. | 雾霾可能是许多细小液体小液滴和固体小颗粒分散到空气中形成的一种胶体 | |
| C. | 铝制餐具不宜用来蒸煮或长时间存放咸的食品 | |
| D. | 在食品袋中放入CaCl2•6H2O,可防止食物受潮 |
| A. | 2.24 L气体是NO | |
| B. | 反应后Fe全部转化为Fe3+ | |
| C. | 反应后的溶液中c(NO3-)=1.7 mol•L-1 | |
| D. | 反应后的溶液最多还能再溶解2.24 g Fe |
| A. | 氧化铜、木炭 | B. | 碳酸钙、碳酸钠 | C. | 氯化铁、氯化钠 | D. | 乙醇、水 |
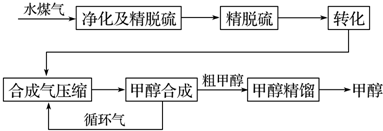
已知:除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成.
(1)制水煤气的主要化学反应方程式为C(s)+H2O(g)?CO(g)+H2(g),此反应是吸热反应.
①此反应的化学平衡常数表达式为$\frac{[CO]•[{H}_{2}]}{[{H}_{2}O]}$;
②下列能提高碳的平衡转化率的措施是BC.
A加入C(s) B.加入H2O(g) C.升高温度 D.增大压强
(2)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为CH4(g)+$\frac{3}{2}$O2(g)?CO(g)+2H2O(g)△H=-519kJ.工业上要选择合适的催化剂,分别对X、Y、Z三种催化剂进行如下实验(其他条件相同).
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是Z(填“X”或“Y”或“Z”),选择的理由是催化活性高、速度快、反应温度较低.
(3)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g)+CO(g)?CH3OH(g)△H=-181.6kJ.4℃下此反应的平衡常数为160.此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/mol•L-1 | 0.2 | 0.1 | 0.4 |
②若加入同样多的CO、H2,在T5℃反应,10min后达到平衡,此时c(H2)=0.4mol•L-1,则该时间内反应速率v(CH3OH)=0.03mol•L-1•min-1.
(4)生产过程中,合成气要进行循环,其目的是提高原料利用率(或提高产量、产率亦可).
 磷及其化合物在生产生活中的用途非常广泛.回答下列问题:
磷及其化合物在生产生活中的用途非常广泛.回答下列问题: