题目内容
1.下列顺序中,错误的是( )| A. | 密度大小:硝基苯>水>苯 | |
| B. | 熔、沸点高低:乙醇>丁烷>丙烷 | |
| C. | 含碳量大小:乙烷>乙醇>乙酸 | |
| D. | 等质量燃烧时的耗氧量:乙烷>乙烯>丙烯 |
分析 A、根据物质的物理性质分析;
B、含有氢键的物质熔沸点较高,分子晶体熔沸点与相对分子质量成正比;
C、乙烷、乙醇和乙酸中均含2个碳原子,但相对分子质量逐渐增大;
D、等质量的烃在燃烧时,H的百分含量越高,则耗氧量越大,据此分析.
解答 解:A、苯的密度小于1g/ml,水的密度等于1g/ml,硝基苯的密度大于1g/ml,所以密度:苯<水<硝基苯,故A正确;
B、含有氢键的物质熔沸点较高,分子晶体熔沸点与相对分子质量成正比,乙醇中含有氢键,熔沸点最高,丙烷相对分子质量大于乙烷且二者都是分子晶体,所以熔沸点:乙醇>丙烷>乙烷,故B正确;
C、乙烷、乙醇和乙酸中均含2个碳原子,但相对分子质量逐渐增大,故从乙烷到乙酸,碳的百分含量逐渐减小,故C正确;
D、等质量的烃在燃烧时,H的百分含量越高,则耗氧量越大,而三种物质中,H的百分含量的关系为乙烷>乙烯=丙烯,故等质量时的耗氧量乙烷>乙烯=丙烯,故D错误.
故选D.
点评 本题考查物质溶解度、熔沸点、密度大小比较,明确分子晶体熔沸点与溶解性的影响因素是解本题关键.

练习册系列答案
相关题目
11.下列离子方程式中不正确的是( )
| A. | 铁粉与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 二氧化碳通入澄清石灰水中CO2+Ca2++2OH-═CaCO3↓+H2O | |
| D. | 氢氧化钡溶液与盐酸混合OH-+H+═H2O |
12. 在100mL0.1mol•L-1铝铵矾[NH4Al(SO4)2•12H2O]的水溶液中,逐滴滴入0.1mol•L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )
在100mL0.1mol•L-1铝铵矾[NH4Al(SO4)2•12H2O]的水溶液中,逐滴滴入0.1mol•L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )
 在100mL0.1mol•L-1铝铵矾[NH4Al(SO4)2•12H2O]的水溶液中,逐滴滴入0.1mol•L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )
在100mL0.1mol•L-1铝铵矾[NH4Al(SO4)2•12H2O]的水溶液中,逐滴滴入0.1mol•L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )| A. | a点溶液中大量存在的离子有NH4+和SO42- | |
| B. | b点溶液中c(NH3•H2O)约为0.1mol•L-1 | |
| C. | a→b过程中,反应的只有SO42- | |
| D. | b→c过程中,反应的是Al(OH)3和NH4+ |
16.下列物质中既能与KMnO4溶液反应、又能与溴水反应的一组物质是( )
①苯 ②乙烯 ③CCl4 ④聚乙烯 ⑤苯乙烯 ⑥已烷.
①苯 ②乙烯 ③CCl4 ④聚乙烯 ⑤苯乙烯 ⑥已烷.
| A. | ②⑤ | B. | ②④⑤ | C. | ②③⑤ | D. | ①②③④⑤⑥ |
10.2008年9月27日,中国航天员首次在太空成功回收了暴露试验的固体润滑材料,这些搭载“神七”飞船的材料共分为4大类15种,这是中国首次暴露于太空环境并成功回收的空间材料试验样品,经过太空的试验以后,以肉眼观察,发现两类产品变化很大,一类是银与银合金的薄膜材料,经过原子氧和紫外光的辐照以后,其表面变花或者变暗;另一类是二硫化钼润滑薄膜产品,表面变得更为粗糙.下列有关说法正确的是( )
| A. | 原子氧比氧气化学性质活泼,二者互为同素异形体 | |
| B. | 银与银合金的薄膜材料化学性质活泼 | |
| C. | 原子氧和紫外光的辐照对二硫化钼润滑薄膜产品没有影响 | |
| D. | 二硫化钼润滑薄膜产品不适合用作航天器的润滑剂 |
10.氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.

(1)根据右侧能量变化示意图1;请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应3A(s)+4B(g)?4C(g)△H>0
其平衡常数K与温度T的关系如下表:
①该反应的平衡常数表达式:K=$\frac{{c}^{4}(C)}{{c}^{4}(B)}$.
②试判断K1<K2(填写“>”,“=”或“<”).
③下列各项能说明该反应已达到平衡状态韵是bd (填字母).
a.容器内B.C的浓度之比为1:1
b.v(B)正=v(C)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度
分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是cd.
a.A、C两点的反应速率:A>C b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在l L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.05mol/L•min.

(1)根据右侧能量变化示意图1;请写出NO2和CO反应的热化学方程式NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(2)在固定体积的密闭容器中,进行如下化学反应3A(s)+4B(g)?4C(g)△H>0
其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②试判断K1<K2(填写“>”,“=”或“<”).
③下列各项能说明该反应已达到平衡状态韵是bd (填字母).
a.容器内B.C的浓度之比为1:1
b.v(B)正=v(C)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)对反应N2O4(g)?2NO2(g)△H>0,在温度
分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示,下列说法正确的是cd.
a.A、C两点的反应速率:A>C b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C d.由状态B到状态A,可以用加热的方法
(4)一定温度下,在l L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的$\frac{7}{8}$,则N2的转化率a(N2)=25%,以NH3表示该过程的反应速率v(NH3)=0.05mol/L•min.
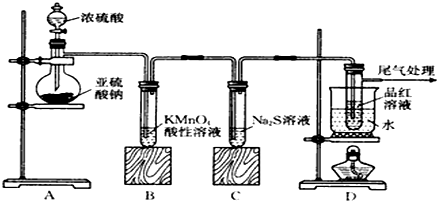
 H2S、金属硫化物是硫的重要化合物.
H2S、金属硫化物是硫的重要化合物.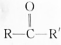 结构);B能与硝酸银的氨溶液作用生成白色沉淀,但C不与之反应.试推测A、B、C的构造式.
结构);B能与硝酸银的氨溶液作用生成白色沉淀,但C不与之反应.试推测A、B、C的构造式.